Bu tez çalışmasının amacı, PEDAS (Precision Epigenetic Delivery and Activation System) sisteminin bitkilerin çoklu stres faktörlerine karşı toleransını artırmadaki etkinliğini ve sürdürülebilir tarıma katkısını kapsamlı olarak değerlendirmektir. Çalışma, epigenetik modülasyon, RNAi/VLP uygulamaları, mikrobiyom mühendisliği ve IoT tabanlı yapay zekâ entegrasyonunu birleştirerek, bitkilerin çevresel streslere karşı önleyici, adaptif ve optimize edilmiş yanıtlar geliştirebileceği bir sistem tasarımını incelemeyi hedeflemektedir.
Temel araştırma soruları:
- Epigenetik programlama ve RNAi/VLP uygulamalarının stres yanıt genleri üzerindeki etkisi nedir?
- Mikrobiyom modülasyonu ve epigenetik müdahale arasındaki sinerji nasıl bir stres toleransı sağlar?
- IoT ve yapay zekâ tabanlı risk tahmini, optimal müdahale stratejilerini nasıl yönlendirir?
- PEDAS sisteminin sürdürülebilir tarıma ve su/kimyasal kullanım etkinliğine katkısı nedir?
GEREÇ VE YÖNTEM
1.Sistem Tasarımı ve Simülasyon
PEDAS modülleri: Epigenetik aktivasyon, RNAi/VLP uygulamaları, mikrobiyom mühendisliği ve IoT-yapay zekâ tabanlı stres tahmin sistemi.
Simülasyon senaryoları: Epigenetik, kontrol, mikrobiyom, RNAi baskılama.
Sensör altyapısı: LoRaWAN ve NB-IoT tabanlı dağıtık sensör ağı, toprak nemi, sıcaklık, pH, EC ölçümleri.
2.Veri Analizi
Betimleyici istatistik: Ortalama, standart sapma, minimum-maksimum değerler.
Normallik ve varyans homojenliği: Artık analizi ve Levene testi.
Tek yönlü ANOVA ve Tukey HSD: Senaryolar arası istatistiksel farkların belirlenmesi.
Korelasyon analizi: Pearson katsayıları, stres-gen ilişkileri.
Temel Bileşenler Analizi (PCA): Çok değişkenli yapı ve senaryo ayrışımı.
Kümeleme analizi: K-Means ile senaryo bazlı gruplaşma.
Zaman serisi analizi: 60 günlük periyotta çevresel stres ve gen ekspresyonu dinamikleri.
Regresyon ve özellik önem analizi: Random Forest ile biyolojik ve çevresel parametrelerin hedef değişkenlere katkısı.
BULGULAR - Epigenetik aktivasyon, gen ekspresyonunu artırırken, RNAi uygulamaları baskılayıcı etki göstermiştir. Kontrol ve mikrobiyom senaryoları yakın değerler göstermiştir.
- Bakteri yoğunluğu, mikrobiyom senaryosunda belirgin şekilde artmıştır; rizosfer modülü simülasyon çıktılarında etkili olmuştur.
- ABA düzeyi, epigenetik ve mikrobiyom senaryolarında anlamlı farklılık göstermiştir.
- Korelasyon analizi, tuz stresi-SOS1, kuraklık-NCED3 ve histon asetilasyonu-stres genleri arasında pozitif, DNA metilasyonu-stres genleri arasında negatif ilişki ortaya koymuştur.
- PCA ve kümeleme analizleri, senaryo bazlı farklılıkların belirgin olduğunu ve sistematik yapı içerdiğini göstermiştir.
- Zaman serisi analizi, çevresel streslerin gen ekspresyon yanıtlarını gecikmeli ve dinamik şekilde tetiklediğini ortaya koymuştur.
- Random Forest regresyon analizi, stres parametreleri, epigenetik değişkenler ve mikrobiyal yoğunluğun sistem davranışında belirleyici olduğunu göstermiştir.
SONUÇ:
PEDAS sistemi, önleyici, adaptif ve parametrize edilebilir bir tarımsal müdahale platformu sunmaktadır.
Epigenetik programlama ve RNAi/VLP uygulamaları ile bitkiler strese hazır hale getirilmektedir.
Mikrobiyom mühendisliği, besin alımı ve abiyotik stres toleransını güçlendirmekte, epigenetik modül ile sinerji oluşturmaktadır.
IoT ve yapay zekâ tabanlı risk tahmini, optimal ve enerji verimli müdahale stratejilerini mümkün kılmaktadır.
Sürdürülebilir tarım açısından, sistem:
Su kullanım etkinliğini %40 artırabilir.
Pestisit/fungisit kullanımını %50-70 azaltabilir.
Toprak sağlığı ve mikrobiyal çeşitliliği iyileştirebilir.
Gelecek çalışmalar, uzun vadeli saha denemeleri, genotip-çevre etkileşimlerinin optimizasyonu, regülasyon uyumu ve kullanıcı adaptasyonu konularında odaklanmalıdır.
1.GİRİŞ VE TEMEL KAVRAMLAR
Geleneksel bitki ıslah programları, strese dayanıklı çeşitlerin geliştirilmesinde önemli başarılar sağlamış olsa da, bu süreçler uzun zaman dilimleri (10–15 yıl) ve yüksek maliyet gerektirmektedir. Genetik modifikasyon (GDO) teknolojileri ise hedef genlere doğrudan müdahale imkânı sunmasına rağmen; kamuoyu algısı, etik tartışmalar ve düzenleyici kısıtlamalar nedeniyle küresel ölçekte sınırlı uygulama alanı bulabilmektedir. Bu bağlamda, kalıcı genom modifikasyonuna başvurmadan, bitkilerin doğal düzenleyici mekanizmalarını aktive eden alternatif yaklaşımlara ihtiyaç duyulmaktadır.
Epigenetik düzenleme mekanizmaları; DNA metilasyonu, histon modifikasyonları, kromatin yeniden şekillenmesi ve küçük RNA aracılı gen susturulması gibi süreçler yoluyla gen ekspresyonunu DNA dizisini değiştirmeksizin kontrol etmektedir. Bitkilerde stres hafızası (priming) fenomeni, epigenetik işaretlerin çevresel koşullara yanıt olarak dinamik biçimde yeniden programlanabildiğini göstermektedir. Bu özellik, epigenetik temelli müdahalelerin hızlı, geri dönüşlü ve potansiyel olarak nesiller arası aktarılabilir avantajlar sağlayabileceğini düşündürmektedir.
Bu tez kapsamında önerilen PEDAS (Precision Epigenetic Delivery and Activation System) platformu; epigenetik programlama, RNAi temelli savunma stratejileri, mikrobiyom mühendisliği, IoT sensör sistemleri ve yapay zekâ destekli karar mekanizmalarını entegre eden çok katmanlı bir biyoteknolojik çerçeve sunmaktadır. Sistem, bitki stres yanıtını genomik düzeyde kalıcı değişiklik yapmadan optimize etmeyi ve çoklu stres koşullarına karşı önceden indüklenmiş dayanıklılık oluşturmayı hedeflemektedir.
Bu yaklaşım, klasik ıslah ile genetik modifikasyon arasında konumlanan, GDO-dışı ancak yüksek hassasiyetli bir müdahale paradigması önermektedir. Böylece sürdürülebilir tarım, biyogüvenlik ve regülasyon uyumu açısından uygulanabilir bir çözüm modeli ortaya konulmaktadır.
Bu çalışmanın temel amacı; bitkilerin doğal epigenetik mekanizmalarını kontrollü ve hedefli biçimde aktive ederek, çoklu abiyotik ve biyotik stres faktörlerine karşı önceden programlanmış dayanıklılık geliştirebilen bütünleşik bir sistem tasarlamak, modellemek ve uygulamaya yönelik fizibilitesini değerlendirmektir.
Bu genel amaç doğrultusunda aşağıdaki alt hedefler belirlenmiştir:
1.Epigenetik Programlama Stratejilerinin Geliştirilmesi:
Kuraklık, tuzluluk ve soğuk gibi temel abiyotik streslere yönelik gen ekspresyon profillerinin epigenetik düzeyde modüle edilmesi için hedef markörlerin belirlenmesi ve müdahale protokollerinin tasarlanması.
2.RNAi Tabanlı Biyotik Savunma Mekanizmalarının Entegrasyonu:
Patojen-spesifik küçük RNA moleküllerinin güvenli taşıyıcı sistemler aracılığıyla bitkiye iletilmesi ve sistemik savunma hafızasının indüklenmesi.
3.Mikrobiyom-Epigenetik Etkileşiminin Modellenmesi:
Rizobakteri ve arbusküler mikoriza (AMF) topluluklarının bitki stres yanıtı üzerindeki etkisinin nicel olarak modellenmesi ve epigenetik düzenleme ile sinerjik ilişkilerinin analiz edilmesi.
4.Gerçek Zamanlı İzleme ve Yapay Zekâ Destekli Karar Mekanizması:
IoT sensörlerinden elde edilen çevresel verilerin makine öğrenmesi algoritmaları ile değerlendirilerek, optimal epigenetik müdahale zamanının belirlenmesi.
5.Simülasyon ve Performans Analizi:
Python tabanlı diferansiyel modelleme yaklaşımıyla sistem dinamiklerinin simüle edilmesi; stres şiddeti, gen ifade düzeyi, mikrobiyal popülasyon değişimi ve verim parametrelerinin birlikte analiz edilmesi.
6.Tekno-Ekonomik ve Biyogüvenlik Değerlendirmesi:
PEDAS platformunun ticari ölçekli uygulamalara uyarlanabilirliğinin analiz edilmesi ve mevcut GDO-dışı düzenlemelerle uyumluluğunun ortaya konulması.
1.1 Araştırmanın Motivasyonu ve Önemi
İklim değişikliği ve artan nüfus baskısı, küresel tarımsal üretimde sürdürülebilir yaklaşımları zorunlu kılmaktadır. Birleşmiş Milletler Gıda ve Tarım Örgütü'nün (FAO) tahminlerine göre, dünya nüfusunun 2050 yılına kadar 9.7 milyara ulaşması beklenmekte ve bu artış, mevcut gıda üretim kapasitesinin %70 oranında artırılmasını gerektirmektedir(FAO, 2017). Ancak mevcut tarımsal alanların genişletilme potansiyeli sınırlıdır ve iklim değişikliğinin getirdiği ekstrem hava olayları, kuraklık ve tuzluluk gibi abiyotik stres faktörleri, tarımsal verimliliği ciddi şekilde tehdit etmektedir(IPCC, 2022).
Küresel su kaynaklarının yaklaşık %70'i tarımda tüketilmektedir(World Bank, 2020) ve dünya genelinde yaklaşık 1,4 milyar hektar alan tuzluluktan etkilenmiş durumdadır(FAO, 2024). Pest kaynaklı kayıplarınsa yüz milyar düzeyinde olduğu ileri sürülmektedir(Pimentel, 2018). Birleşmiş Milletler Gıda ve Tarım Örgütü'ne göreyse, küresel mahsul üretiminin %40'a kadarı bitki zararlıları ve hastalıkları nedeniyle kaybediliyor(WEF, 2021). İklimsel dalgalanmaların bitki büyümesi ve gelişiminde oluşturduğu verim düşüşleri, gıda güvenliğini doğrudan tehdit etmektedir(Boyer, 2019). Bu bağlamda, bitkilerin abiyotik ve biyotik stres faktörlerine karşı dayanıklılığını artırmak, sürdürülebilir tarım için kritik bir öneme sahiptir(Zhu, 2016).
Geleneksel ıslah programları, strese dayanıklı bitki çeşitlerinin geliştirilmesinde önemli başarılar elde etmiş olsa da, bu süreçler genellikle 10-15 yıl gibi uzun zaman gerektirmekte ve yüksek maliyetlerle gerçekleşmektedir. Genetik modifikasyon (GDO) teknolojileri ise daha hızlı sonuçlar vaat etmekle birlikte, kamuoyu direnci, etik kaygılar ve katı yasal düzenlemeler nedeniyle sınırlı bir uygulama alanına sahiptir. Özellikle Avrupa Birliği ve birçok gelişmekte olan ülkede GDO'ya yönelik kısıtlayıcı politikalar, bu teknolojilerin yaygın kullanımını engellemektedir(FAO, 2021).
Bu tez; bitkilerin genetik koduna kalıcı müdahale etmeden, doğal epigenetik mekanizmaları kontrollü bir biçimde aktive ederek hızlı, geri dönüşlü ve sürdürülebilir bir çözüm sunmayı amaçlamaktadır. PEDAS (Precision Epigenetic Delivery and Activation System) sistemi, biyoteknoloji, nanoteknoloji, mikrobiyom mühendisliği ve yapay zeka teknolojilerini entegre ederek, tarımsal üretimde paradigma değişimine öncülük edebilecek yenilikçi bir platformdur(Trivedi et al., 2020).
Önerilen PEDAS sistemi, bitki stres yanıt mekanizmaları ve mikrobiyom etkileşimlerinin zamana bağlı değişimini modellemek amacıyla Python programlama dili kullanılarak simüle edilmiştir. Python tercih edilmesinin temel nedenleri; bilimsel hesaplama kütüphanelerinin yaygın kullanımı, veri işleme kapasitesi ve görselleştirme olanaklarının güçlü olmasıdır.
Simülasyon modeli, bitki stres dinamiklerini temsil eden diferansiyel süreçler, gen ifade değişimleri ve rizosfer mikrobiyal popülasyon etkileşimlerini birlikte değerlendiren modüler bir yapı üzerine kurulmuştur. Model, zaman adımları üzerinden ilerleyen iteratif bir hesaplama yaklaşımıyla çalışmaktadır.
Kod yapısı genel olarak aşağıdaki bileşenlerden oluşmaktadır:
Çevresel stres parametrelerinin tanımlandığı başlangıç modülü,
Epigenetik düzenleme ve gen ifade mekanizmalarını temsil eden hesaplama fonksiyonları,
Rizobakteri ve arbusküler mikoriza (AMF) popülasyon değişimlerini modelleyen mikrobiyom modülü,
Yapay zekâ destekli karar mekanizması ile müdahale gereksinimlerinin belirlenmesi,
Sonuçların grafiksel olarak görselleştirilmesi ve raporlanması.
Simülasyonlar belirli zaman aralıklarında çevresel stres koşullarının değiştiği senaryolar altında yürütülmüş ve elde edilen çıktılar grafikler ve performans göstergeleri şeklinde değerlendirilmiştir.
Bu çalışmada kullanılan Python kodları tez metninin akışını bozmamak amacıyla ana metin içerisinde verilmemiş olup, çalışmanın yeniden üretilebilirliğini sağlamak amacıyla Ekler bölümünde sunulmuştur.
Tezin yazım sürecinde, fikirsel içerik ve akademik yapı yazara ait olmak kaydıyla, dil ve teknik yazım denetimi amacıyla ChatGPT isimli yapay zekâ aracından destek alınmıştır.
1.2 Epigenetik: Temel Kavramlar ve Mekanizmalar
Epigenetik, DNA diziliminde değişiklik yapmadan gen ekspresyonunu düzenleyen kalıtsal veya edinilmiş fizikokimyasal modifikasyonları inceleyen bilim dalıdır. "Epigenetik" terimi, Yunanca "epi" (üzerinde, ötesinde) ve "genetik" kelimelerinin birleşiminden oluşur ve genetik bilginin nasıl okunduğunu ve yorumlandığını kontrol eden mekanizmaları ifade eder. Conrad Waddington tarafından 1942 yılında ortaya atılan bu kavram, günümüzde moleküler biyolojinin en dinamik araştırma alanlarından biri haline gelmiştir(Waddington, 1942; Bird, 2007).
1.2.1 DNA metilasyonu
DNA metilasyonu, sitozin bazlarının 5. karbon atomuna metil gruplarının (CH₃) kovalent bağlanması işlemidir. Bu modifikasyon, özellikle sitozin-guanin dinükleotid (CpG) bölgelerinde yoğunlaşır(Law & Jacobsen, 2010). Bitkilerde DNA metilasyonu üç farklı bağlamda gerçekleşir:
- CpG (CG) metilasyonu: Genellikle gen promotör bölgelerinde bulunur ve gen susturulmasıyla ilişkilidir. DNA metiltransferaz 1 (MET1) enzimi tarafından katalize edilir.
- CHG metilasyonu: H herhangi bir baz (A, T veya C) olabilir. Kromatometin Metilaz 3 (CMT3) enzimi tarafından düzenlenir.
- CHH metilasyonu: Asymmetric metilasyon olarak da bilinir ve Domains Rearranged Methyltransferase 2 (DRM2) tarafından yönetilir(Zhang, Lang & Zhu, 2018).
DNA metilasyonu, transkripsiyon faktörlerinin DNA'ya bağlanmasını engelleyerek veya metil-CpG bağlayıcı protein komplekslerini (MBD proteinleri) toplayarak gen ifadesini baskılar. Bitkilerde stres koşulları altında metilasyon paternlerinde dinamik değişiklikler gözlenir ve bu değişiklikler stres hafızasının oluşmasında kritik rol oynar.(Chinnusamy & Zhu, 2009).
1.2.2 Histon modifikasyonları
Histonlar, DNA'nın sarıldığı protein yapılardır ve nükleozom adı verilen temel kromatin birimini oluştururlar. Her nükleozom, iki kopyadan oluşan dört çekirdek histon proteininden (H2A, H2B, H3, H4) oluşur ve etrafına yaklaşık 147 baz çifti DNA sarılır(Luger et al., 1997) Histon proteinlerinin N-terminal kuyruk bölgeleri, çeşitli posttranslasyonel modifikasyonlara uğrayabilir(Kouzarides, 2007):
- Histon Asetilasyonu: Lisin aminoasitlerine asetil gruplarının eklenmesi, kromatin yapısını gevşetir ve gen transkripsiyonunu aktive eder. Histon asetiltransferazlar (HAT) bu reaksiyonu katalize ederken, histon deasetilazlar (HDAC) ters reaksiyonu gerçekleştirir. H3K9ac (Histon 3, 9. pozisyon lisin asetilasyonu) ve H3K14ac gibi markörler aktif gen ifadesiyle ilişkilidir(Bannister & Kouzarides, 2011).
- Histon Metilasyonu: Lisin veya arginin rezidülerine metil gruplarının eklenmesi. Metilasyon durumuna (mono-, di- veya tri-metilasyon) ve pozisyonuna bağlı olarak farklı etkiler gösterir. H3K4me3 (Histon 3, 4. pozisyon lisin tri-metilasyonu) aktif gen promotörlerinde bulunurken, H3K27me3 ve H3K9me3 gen susturulmasıyla ilişkilidir(Kouzarides, 2007).
- Histon Fosforilasyonu: Serin, treonin veya tirozin rezidülerine fosfat gruplarının eklenmesi. DNA hasar yanıtı ve hücre döngüsü düzenlemesinde rol oynar.(Rossetto et al., 2012)
- Histon Ubikuitinasyonu: Ubikuitin proteinlerinin lizin rezidülerine konjugasyonu. H2Bub1 (H2B mono-ubikuitinasyonu) transkripsiyon elongasyonunda önemlidir(Weake & Workman, 2008).
Bu modifikasyonlar, "histon kodu hipotezi" olarak bilinen kompleks bir düzenleme sistemini oluşturur. Farklı histon modifikasyonlarının kombinasyonu, spesifik gen ifade profillerini belirler ve hücresel fonksiyonları yönlendirir(Strahl & Allis, 2000).
1.2.3 Kromatin yeniden şekillenmesi
Kromatin yeniden şekillendirme kompleksleri (CRC'ler), ATP hidrolizinden elde edilen enerjiyi kullanarak nükleozom pozisyonlarını değiştiren protein yapılarıdır. SWI/SNF, ISWI, CHD ve INO80 aileleri gibi farklı CRC aileleri, nükleozomların kaymasını, yerinden çıkarılmasını veya DNA üzerinde yeniden konumlandırılmasını sağlar. Bu süreç, transkripsiyon faktörlerinin ve diğer düzenleyici proteinlerin DNA'ya erişimini kontrol ederek gen ifadesini düzenler(Clapier & Cairns, 2009).
1.2.4 Küçük RNA'lar ve RNA susturulması
Küçük RNA molekülleri, özellikle mikroRNA'lar (miRNA) ve küçük interferans RNA'lar (siRNA), post-transkripsiyonel gen susturulmasında kritik roller oynar(Mladenov et al., 2021):
- miRNA'lar: 20-24 nükleotid uzunluğunda endojen RNA molekülleridir. Bitkide MIR genleri tarafından kodlanır ve hedef mRNA'larının translasyonunu baskılar veya degradasyonunu tetikler. Stres yanıtlarında düzenleyici roller üstlenir.
- siRNA'lar: Çift zincirli RNA'lardan (dsRNA) üretilen 21-24 nükleotid uzunluğundaki moleküllerdir. RNA Induced Silencing Complex (RISC) ile birleşerek hedef RNA'ları parçalar. Bitkilerde viral enfeksiyonlara karşı savunmada önemli rol oynar.
- RNA-directed DNA Methylation (RdDM): Bitkilere özgü bir mekanizmadır. 24-nükleotid siRNA'lar, DRM2 metiltransferazı kompleksini spesifik genomik bölgelere yönlendirerek DNA metilasyonunu indükler. Bu süreç, transpozon susturulması ve genomik stabilite için kritiktir(Mladenov et al., 2021).
1.3 Bitkilerde Stres Hafızası ve Epigenetik Düzenleme
Bitkiler, geçmiş stres deneyimlerini "hatırlayabilir" ve benzer streslerle tekrar karşılaştıklarında daha hızlı ve güçlü yanıtlar verebilir. Bu fenomen "stres hafızası" veya "priming" olarak adlandırılır ve epigenetik mekanizmalar tarafından yönetilir. Epigenetik stres hafızası, gen ekspresyonunda kalıcı olmayan ancak yeniden aktive edilebilir değişiklikler oluşturarak bitkilerin çevresel dalgalanmalara uyum kapasitesini artırmaktadır (Mladenov et al., 2021).
1.3.1 Stres hafızasının moleküler temelleri
Stres hafızası üç temel kategoriye ayrılır(Zhu, 2016; Mladenov et al., 2021):
- Somatik Hafıza: Aynı bireyin yaşamı boyunca tutulan hafızadır. Örneğin, kuraklık stresi yaşamış bir bitki, ikinci kuraklık olayında daha hızlı stoma kapanması ve osmoprotektan üretimi gösterebilir.
- İntrajenereasyonel Hafıza: Aynı generasyonda farklı gelişim evrelerinde aktarılan hafızadır. Fide döneminde yaşanan soğuk stresi, çiçeklenme dönemindeki soğuğa toleransı artırabilir.
- Transjenereasyonel Hafıza: Ebeveyn bitkiden yavrulara aktarılan epigenetik bilgidir. Meiotik bölünmeler sırasında çoğu epigenetik işaret silinse de, bazı markörler (özellikle bazı DNA metilasyon paternleri ve bazı histon modifikasyonları) nesiller arası aktarılabilir(Mladenov et al., 2021).
1.3.2 Stres yanıtında epigenetik değişiklikler
Kuraklık stresi altında, Arabidopsis thaliana'da RD29A (Responsive to Desiccation 29A) ve RD22 gibi kuraklık yanıt genlerinin promotör bölgelerinde DNA demetilasyonu ve H3K4me3 artışı gözlenir. Bu değişiklikler, genlerin hızlı transkripsiyonunu mümkün kılar(Zhu, 2016). Benzer biçimde tuz stresi altında, SOS (Salt Overly Sensitive) sinyal yolağında görev alan genlerde histon asetilasyon paternlerinde dinamik değişimler gözlenmiştir ve bu değişimler iyon homeostazının düzenlenmesine katkı sağlar (Zhu, 2016).
Soğuk stresi yanıtında, CBF (C-repeat Binding Factor) transkripsiyon faktörlerinin ekspresyonunu düzenleyen epigenetik mekanizmalar özellikle önemlidir. Vernalizasyon (soğuklaşma) sürecinde, FLC (Flowering Locus C) geninin susturulması H3K27me3 metilasyonundaki artışla gerçekleşir ve bu susturulma çiçeklenme zamanlamasını kontrol eder(Mladenov et al., 2021).
1.3.3 Biyotik stres ve epigenetik
Patojen enfeksiyonları sonrasında, bitkilerde Systemic Acquired Resistance (SAR) adı verilen uzun süreli savunma hafızası oluşabilir. Bu süreçte, NPR1 (Nonexpressor of Pathogenesis-Related genes 1) ve PR (Pathogenesis-Related) genlerinde kromatin modifikasyonları gerçekleşir. H3K4me2/me3 artışı ve H3K9ac zenginleşmesi, bu genleri "hazır" durumda tutar ve ikincil enfeksiyonlarda daha hızlı savunma yanıtı sağlar(Mladenov et al., 2021)
1.4 Araştırmanın Hipotezi ve Hedefleri
Bu tezin temel hipotezi şudur: Bitkilerin doğal epigenetik mekanizmaları, eksternal müdahalelerle kontrollü biçimde programlanarak, çoklu stres faktörlerine karşı dayanıklılık önceden indüklenebilir ve bu indüksiyon, bitki performansında ölçülebilir iyileşmeler sağlayabilir.
Araştırmanın Spesifik Hedefleri:
- Kuraklık, tuzluluk ve soğuk gibi abiyotik streslere yönelik epigenetik programlama stratejilerinin geliştirilmesi.
- Patojen spesifik RNAi tabanlı savunma sistemlerinin virüs benzeri partiküller (VLP) kullanılarak bitkilere iletilmesi.
- Bitki kök bölgesinde stres toleransını artıran faydalı mikrobiyom topluluklarının kurulması ve mikrobiyom-epigenetik etkileşimlerinin karakterizasyonu.
- IoT sensörleri ve yapay zeka algoritmaları kullanılarak, gerçek zamanlı stres tespiti ve otomatik epigenetik müdahale protokollerinin oluşturulması.
- Geliştirilen PEDAS sisteminin ticari çiftlik koşullarında pilot uygulamalarının gerçekleştirilmesi ve tekno-ekonomik analizinin yapılması.
- Sistemin biyogüvenlik profilinin değerlendirilmesi ve mevcut GDO-dışı düzenlemelere uyumluluğunun doğrulanması.
1.5 Tezin Yapısı ve Organizasyonu
Bu tez dokuz ana bölümden oluşmaktadır. Giriş bölümünün ardından, ikinci bölümde bitkilerde stres mekanizmaları ve mevcut epigenetik araştırmalar kapsamlı olarak incelenecektir. Üçüncü bölüm PEDAS sisteminin çekirdek teknolojisi olan epigenetik programlama modülünün detaylarını sunacaktır. Dördüncü bölümde RNAi ve mikrobiyom entegrasyonu ele alınacak, beşinci bölümde IoT ve yapay zeka uygulamaları tartışılacaktır. Altıncı bölüm hukuki statü ve regülasyon konularına odaklanacak, yedinci bölüm materyal, yöntem ve bulgular, sekizinci bölüm ekonomik analiz ve ticarileşme stratejisi, son bölümde ise genel değerlendirme ve gelecek perspektifler sunulacaktır.
2. MEVCUT DURUM VE İLGİLİ ÇALIŞMALAR
2.1 Bitkilerde Stres Mekanizmaları
Bitkilerin stres faktörlerine verdiği yanıtlar, karmaşık ve çok katmanlı moleküler süreçlerle yönetilir. Bu süreçler genel olarak üç ana aşamada gerçekleşir: stres algılama, sinyal transdüksiyonu ve adaptif yanıtların aktivasyonu(Zhu, 2016; Taiz et al., 2015).
2.1.1. Abiyotik stres algılama ve sinyal iletimi
Kuraklık Stresi:
Kuraklık stresi, bitkilerin karşılaştığı en yaygın ve tahripkar abiyotik stres faktörlerinden biridir. Su eksikliği, hücre turgor basıncında düşüşe, fotosentetik aktivitede azalmaya ve nihayetinde büyüme geriliğine yol açar. Kuraklık algılama, plazma membranında bulunan osmosensörler ve mekanosensitif iyon kanalları aracılığıyla gerçekleşir. Bu reseptörler, hücre içi kalsiyum (Ca²⁺) konsantrasyonunda ani artışları tetikler(Zhu, 2016).
Absisik asit (ABA), kuraklık yanıtının merkezi düzenleyicisidir. Kök ve yaprak hücrelerinde üretilen ABA, stoma kapanmasını indükler ve su kaybını minimuma indirir. ABA sinyallemesi, PYR/PYL/RCAR reseptör ailesi, PP2C fosfatazları ve SnRK2 kinazları arasındaki etkileşimlerle düzenlenir. ABA varlığında, PYR reseptörleri PP2C fosfatazlarını inhibe eder ve bu durumsa SnRK2 kinazlarının aktif kalmasını sağlar. Aktif SnRK2 kinazları, transkripsiyon faktörlerini (ABF/AREB, MYB, NAC ve WRKY aileleri) fosforile ederek kuraklık yanıt genlerinin ekspresyonunu indükler(Cutler et al., 2010; Zhu, 2016).
Kuraklık yanıt genleri arasında:
-Osmoprotektan sentez genleri: Prolin, glisin betain, trehaloz gibi moleküllerin üretimini kodlar.
-LEA proteinleri (Late Embryogenesis Abundant): Hücre membranlarını ve proteinleri korur.
-Aquaporinler (PIP, TIP, NIP aileleri): Su transportunu düzenler.
-Detoksifikasyon enzimleri: Reaktif oksijen türlerini (ROS) temizler(Taiz et al., 2015).
Tuzluluk Stresi:
Tuzluluk stresi, hem ozmotik hem de iyonik stres bileşenlerine sahiptir. Yüksek toprak tuzluluğu (özellikle NaCl), su alımını zorlaştırır (ozmotik stres) ve hücre içinde toksik iyon birikimine (özellikle Na⁺ ve Cl⁻) neden olur (iyonik stres)(Zhu, 2016).
SOS (Salt Overly Sensitive) yolu, tuz toleransının ana düzenleyicisidir. Bu yolun ana bileşenleri:
-SOS3: Tuz stresiyle oluşan kalsiyum stresini algılayan sensör protein.
-SOS2: SOS3 tarafından aktif edilen bir protein kinazdır ve sinyal iletimini sürdürür.
-SOS1: Hücre zarındaki bir taşıyıcı olup fazla sodyumu hücre dışına atarak iyon dengesini sağlar.
Tuz stresi altında artan sitosolik Ca²⁺ seviyeleri, SOS3'ü aktive eder. SOS3-SOS2 kompleksi, SOS1'i fosforile ederek Na⁺'nın hücre dışına atılmasını sağlar. Ayrıca, vakuolar Na⁺/H⁺ antiporterleri (NHX ailelesi) Na⁺'nın vakuol içinde sekestre edilmesini sağlar ve sitoplazmadaki toksik iyonu azaltır.(Zhu, 2016; Taiz et al., 2015)
Soğuk Stresi:
Soğuk stresi, membran fluiditesinde azalma, protein denatürasyonu ve metabolik reaksiyonlarda yavaşlamaya neden olur. Bitkiler, soğuk stresi yanıtını ICE (Inducer of CBF Expression) - CBF/DREB1 - COR (Cold Regulated) genetik kaskadı üzerinden düzenler.
Düşük sıcaklıklar, membran rijiditesini artırarak Ca²⁺ kanallarının açılmasını tetikler. Artan Ca²⁺ seviyeleri, ICE1 transkripsiyon faktörünü aktive eder. ICE1, CBF/DREB1 genlerinin promotörlerine bağlanarak ekspresyonlarını indükler. CBF proteinleri ise COR genlerin promotörlerindeki CRT/DRE (C-repeat/Dehydration-Responsive Element) bölgelerine bağlanarak soğuk toleransı sağlayan proteinlerin üretimini başlatır(Chinnusamy et al., 2007; Zhu, 2016).
Isı Stresi:
Yüksek sıcaklıklar, protein katlanma hatalarına ve agregasyona yol açar. Isı şok proteinleri (HSP), yanlış katlanmış proteinlerin düzeltilmesinde veya degradasyonunda görev alır. Isı şok faktörleri (HSF), HSP genlerinin transkripsiyonunu düzenleyen ana transkripsiyon faktörleridir(Bokszczanin & Fragkostefanakis, 2013).
2.1.2 Biyotik stres yanıtları
Bitkilerin patojen enfeksiyonlarına karşı savunması, pattern-triggered immunity (PTI) ve effector-triggered immunity (ETI) olmak üzere iki katmanlı bir sistemle gerçekleşir(Jones ve Dangl, 2006).
Pattern-Triggered Immunity (PTI):
Bitki hücreleri, pathogen-associated molecular patterns (PAMP) olarak adlandırılan korunmuş mikrobiyal yapıları tanıyan pattern recognition receptors (PRR) içerir (Zipfel, 2008). Örneğin, FLS2 reseptörü bakteriyel flagellin proteinini (Gómez-Gómez ve Boller, 2000), EFR reseptörü ise bakteriyel elongation factor Tu'yu (EF-Tu) tanır (Zipfel ve ark., 2006). PAMP algılama, MAP kinaz (MAPK) kaskadlarının aktivasyonunu tetikler (Asai ve ark., 2002) ve savunma genlerinin ekspresyonunu indükler.
Effector-Triggered Immunity (ETI):
Patojenler, bitki savunmasını bastırmak için efektör proteinleri salgılarlar. Bitkiler, bu efektörleri resistance (R) proteinleri aracılığıyla tanır. R proteinleri genellikle NB-LRR (nucleotide-binding leucine-rich repeat) yapısına sahiptir (Dangl ve Jones, 2001). Efektör tanıma, güçlü ve hızlı bir savunma yanıtını tetikler ve genellikle hipersensitif yanıt (HR) adı verilen programlı hücre ölümü ile sonuçlanır (Coll ve ark., 2011).
Hormon Sinyal Ağları:
Biyotik stres yanıtları, hormon sinyal ağlarıyla düzenlenir (Pieterse ve ark., 2009):
-Salisilik asit (SA): Biyotrofik ve hemibiyotrofik patojenlere karşı savunmada merkezi rol oynar. SAR (Systemic Acquired Resistance) oluşumunda kritiktir (Durrant ve Dong, 2004).
-Jasmonik asit (JA): Nekrotrofik patojenlere ve otçul böceklere karşı savunmada önemlidir (Howe ve Jander, 2008).
-Etilen (ET): JA ile sinerjistik olarak çalışır ve yaşlanma ile stres yanıtlarını düzenler (Broekaert ve ark., 2006).
SA ve JA yolakları genellikle antagonistik ilişki gösterir; bir yolağın aktivasyonu diğerini baskılar (Thaler ve ark., 2012). Bu antagonizma, bitkilerin kaynakları en uygun şekilde tahsis etmesini sağlar.
2.1.3 Stres yanıtlarının zaman dinamikleri
Bitkilerin stres yanıtları, çeşitli zaman ölçeklerinde gerçekleşir (Atkinson ve Urwin, 2012; Skirycz ve Inzé, 2010):
1.Erken Yanıtlar (0-30 dakika): İyon akışları, ROS üretimi, protein fosforilasyonu (Boller ve Felix, 2009).
2.Orta Vadeli Yanıtlar (30 dakika - 6 saat): Gen ekspresyonu değişiklikleri, hormon sentezi (Hickman ve ark., 2017).
3.Geç Yanıtlar (6-48 saat): Metabolik yeniden programlama, büyüme ayarlamaları (Windram ve ark., 2012).
4.Uzun Vadeli Adaptasyon (günler-haftalar): Morfolojik değişiklikler, gelişimsel modifikasyonlar.
Klasik stres yanıtlarının önemli bir dezavantajı, stresin başlangıcı ile adaptif yanıtların tam olarak devreye girmesi arasında geçen 2-6 saatlik gecikme süresidir (Conrath, 2011). Bu gecikme, bitkilerin kritik ilk saatlerde strese karşı savunmasız kalmasına neden olur. PEDAS sistemi, epigenetik ön-programlama yoluyla bu gecikme süresini ortadan kaldırmayı hedefler (Bruce ve ark., 2007). Stres yanıt genleri önceden "hazır" durumda tutularak, stres algılandığı anda hemen aktive edilebilir hale getirilir.
2.2 Epigenetik Araçlar ve Teknolojiler
2.2.1 DNA metilasyonu: moleküler mekanizmalar ve fonksiyonlar
DNA metilasyonu, genomdaki en iyi karakterize edilmiş epigenetik işarettir (Law ve Jacobsen, 2010). Bitkilerde, DNA metilasyonu üç ana DNA metiltransferaz (DNMT) ailesi tarafından katalize edilir (Cao ve Jacobsen, 2002; Henderson ve Jacobsen, 2007).
DNA Methyltransferase 1 (MET1):
MET1, memelilerdeki DNMT1'in homologudur ve hemi-metile CpG dizilerini tanıyarak yeni sentezlenen DNA zincirine metil grupları aktarır. Bu enzim, DNA replikasyonu sırasında metilasyon paternlerinin korunmasını (maintenance methylation) sağlar (Kankel ve ark., 2003; Saze ve ark., 2003). MET1'in aktivitesi, VIM (Variant in Methylation) proteinleri tarafından düzenlenir (Woo ve ark., 2008).
Chromomethylase 3 (CMT3) ve CMT2:
CMT3, CHG bağlamındaki metilasyonu katalize eder ve H3K9me2 histon markörü ile etkileşim halindedir (Lindroth ve ark., 2001; Du ve ark., 2012). CMT2 ise CHH metilasyonundan sorumludur ve heterokromatik bölgelerde yoğunlaşır (Zemach ve ark., 2013; Stroud ve ark., 2014). Bu enzimler, DNA metilasyonu ile histon modifikasyonları arasında bir köprü oluşturarak, epigenetik düzenlemelerin entegrasyonunu sağlar.
Domains Rearranged Methyltransferase 2 (DRM2):
DRM2, memelilerdeki DNMT3 ailesinin fonksiyonel homologudur ve de novo (yeni) metilasyonu gerçekleştirir (Cao ve Jacobsen, 2002). RNA-directed DNA Methylation (RdDM) yolağında merkezi bir rol oynar (Matzke ve Mosher, 2014). 24-nükleotid siRNA'lar, AGO4 proteini ve NRPE1 (RNA Polimeraz V) ile etkileşime girerek DRM2'yi belirli genomik lokalizasyonlara yönlendirir (Wierzbicki ve ark., 2009; Zhong ve ark., 2014).
DNA Demetilasyon:
DNA demetilasyonu, aktif bir süreçtir ve base excision repair (BER) mekanizmasıyla gerçekleşir (Zhu, 2009). Bitkilerde dört ROS (Repressor of Silencing) / DME (Demeter) ailesi glikozilaz proteini bulunur (Ortega-Galisteo ve ark., 2008):
-DME: Merkezi hücrede ve endospermde eksprese edilir (Choi ve ark., 2002).
-ROS1: Vejetatif dokularda yaygın ekspresyon gösterir (Gong ve ark., 2002).
-DML2 ve DML3: Daha spesifik ekspresyon paternlerine sahiptir (Penterman ve ark., 2007).
Bu enzimler, 5-metilsitozini baz olarak tanıyıp çıkarır ve BER yoluyla metillenmemiş sitozinle değiştirir (Agius ve ark., 2006). Aktif demetilasyon, dinamik gen düzenlemesinde ve stres yanıtlarında kritik öneme sahiptir (Le ve ark., 2014).
2.2.2 Histon modifikasyonları: "histon kodu" ve fonksiyonel sonuçları
Histon modifikasyonları, kromatin yapısını ve transkripsiyon makinasının DNA'ya erişimini düzenleyen kompleks bir sinyal ağı oluşturur. Farklı histon modifikasyonlarının kombinasyonu, spesifik biyolojik sonuçlar doğurur ve bu kavram "histon kodu hipotezi" olarak formüle edilmiştir (Jenuwein ve Allis, 2001; Strahl ve Allis, 2000).
Aktif Kromatin Markerleri:
1.H3K4me3 (Histon H3, Lizin 4, Tri-metilasyon):
-Aktif gen promotörlerinde zenginleşir (Zhang ve ark., 2009).
-Transkripsiyon başlangıç kompleksinin (pre-initiation complex) oluşumunu destekler.
-SET1/COMPASS kompleksi tarafından katalize edilir (Fromm ve Avramova, 2014).
-Transcription factor IID (TFIID) ve chromatin remodeling faktörler tarafından tanınır (Vermeulen ve ark., 2007).
2.H3K9ac (Histon H3, Lizin 9, Asetilasyon):
-Kromatin yapısını gevşetir ve nükleozom-DNA etkileşimini zayıflatır (Eberharter ve Becker, 2002).
-Histon asetiltransferazlar (HAT), özellikle GCN5 ve CBP/p300 aileleri tarafından katalize edilir (Pandey ve ark., 2002).
-Aktif transkripsiyon ile güçlü korelasyon gösterir (Benhamed ve ark., 2006).
3.H3K36me3:
-Gen gövdesinde (gene body) zenginleşir (Oh ve ark., 2008).
-Transkripsiyon elongasyonu sırasında oluşur.
- Spurious transkripsiyon başlangıçlarını önler (Carrozza ve ark., 2005).
Represif Kromatin Markerleri:
1.H3K27me3:
-Polycomb Repressive Complex 2 (PRC2) tarafından katalize edilir (Schuettengruber ve ark., 2007).
- Gelişimsel olarak düzenlenen genlerin susturulmasında kritik rol oynar (Makarevich ve ark., 2006).
-Facultative heterochromatin oluşumunda merkezi öneme sahiptir (Turck ve ark., 2007).
2.H3K9me2/me3:
-Konstitutif heterokromatin markeridir (Jackson ve ark., 2002).
-Transpozon ve tekrar dizilerinin susturulmasında önemlidir (Lippman ve ark., 2004).
-Su(var)3-9 metiltransferazları tarafından katalize edilir (Malagnac ve ark., 2002).
-HP1 (Heterochromatin Protein 1) proteinlerini toplar ve kromatin kondensasyonunu indükler (Fischle ve ark., 2005).
Histon Modifikasyonu Yazıcıları, Silicileri ve Okuyucuları:
Histon modifikasyonları sistemini üç protein sınıfı düzenler (Kouzarides, 2007):
-Yazıcılar (Writers): Modifikasyonları ekleyen enzimler (HAT, HMT, protein kinazlar).
-Siliciler (Erasers): Modifikasyonları kaldıran enzimler (HDAC, HDM, fosfatazlar).
-Okuyucular (Readers): Modifikasyonları tanıyan proteinler (bromodomain, chromodomain, PHD finger içeren proteinler; Liu ve ark., 2014; Yun ve ark., 2012).
2.2.3RNA interferans (RNAi): mekanizmalar ve uygulamalar
RNA interferans, çift zincirli RNA (dsRNA) tarafından tetiklenen sekans-spesifik gen susturulması mekanizmasıdır (Fire ve ark., 1998). Bitkilerde, RNAi doğal olarak viral enfeksiyonlara karşı savunmada ve genomik stabilitenin korunmasında görev alır (Waterhouse ve ark., 2001; Baulcombe, 2004).
RNAi Mekanizmasının Aşamaları:
1.dsRNA Tanıma ve İşleme:
- Dicer-like (DCL) enzimleri, uzun dsRNA moleküllerini 21-24 nükleotid uzunluğunda küçük RNA'lara (siRNA) keser (Bernstein ve ark., 2001; Hamilton ve Baulcombe, 1999).
-Bitkilerde dört DCL proteini bulunur (DCL1-4), her biri farklı küçük RNA türlerini üretir (Schauer ve ark., 2002; Xie ve ark., 2004).
-DCL1: miRNA üretiminde özel görev alır (Kurihara ve Watanabe, 2004).
-DCL2-4: siRNA üretiminde farklı biyolojik bağlamlarda çalışır (Bouche ve ark., 2006; Deleris ve ark., 2006).
2.RISC Kompleksinin Oluşumu:
-Küçük RNA'lar, Argonaute (AGO) proteinleriyle kompleks oluşturur (Hammond ve ark., 2001).
-Bitkilerde 10 AGO proteini bulunur (AGO1-10) (Morel ve ark., 2002; Vaucheret, 2008).
-AGO proteini, küçük RNA'nın "guide strand"ini tutar, "passenger strand"i ise atılır (Matranga ve ark., 2005).
3.Hedef RNA'nın Tanınması ve Susturulması:
-Guide strand, komplementer hedef mRNA'ya hibridize olur.
-AGO1, tam komplementer hedefleri endonükleolitik olarak keser (slicing) (Baumberger ve Baulcombe, 2005).
-Kısmi komplementarite durumunda, translasyon inhibisyonu veya mRNA degradasyonu gerçekleşir (Brodersen ve ark., 2008).
RNA Yönlendirmeli DNA Metilasyonu (RNA-directed DNA Methylation - RdDM):
RdDM, bitkilere özgü bir mekanizmadır ve siRNA'ların DNA metilasyonunu yönlendirmesini sağlar (Matzke ve ark., 2009; Law ve Jacobsen, 2010):
1.RNA Polimeraz IV (Pol IV), transkriptler (scaffold RNA) üretir (Herr ve ark., 2005; Onodera ve ark., 2005).
2.RNA-dependent RNA polymerase 2 (RDR2), bu transkriptleri dsRNA'ya dönüştürür (Xie ve ark., 2004).
3.DCL3, dsRNA'yı 24-nükleotid siRNA'lara keser (Xie ve ark., 2004; Henderson ve ark., 2006).
4.AGO4, siRNA'yı tanır ve RNA Polimeraz V (Pol V) transkriptleri ile etkileşime girer (Wierzbicki ve ark., 2008; Wierzbicki ve ark., 2009).
5.DRM2, AGO4-siRNA-Pol V kompleksi tarafından yönlendirilerek hedef bölgeyi metile eder (Cao ve Jacobsen, 2002; Zhong ve ark., 2014).
Bu mekanizma, transpozon susturulmasında, heterokromatin oluşumunda ve stres yanıtlarının epigenetik düzenlemesinde kritik rol oynar (Lippman ve ark., 2004; Dowen ve ark., 2012).
2.2.4Kromatin immünopresipitasyonu ve epigenom haritalama
Epigenetik modifikasyonların genom çapında haritalanması, modern epigenetik araştırmaların temelini oluşturur (Furey, 2012). Kullanılan başlıca teknolojiler:
ChIP-seq (Chromatin Immunoprecipitation Sequencing):
-Spesifik histon modifikasyonlarına veya transkripsiyon faktörlerine karşı antikorlar kullanarak, bu proteinlerin bağlı olduğu DNA bölgelerini izole eder (Johnson ve ark., 2007; Barski ve ark., 2007).
-Yüksek çözünürlükte genom çapında lokalizasyon haritaları oluşturur (Park, 2009).
-Stres koşulları altında epigenetik değişikliklerin dinamiklerini incelemek için kullanılır (Kim ve ark., 2008; Zhang ve ark., 2007).
Bisülfit Sekanslama:
-DNA'daki metillenmiş sitozinlerin haritalanmasında altın standarttır (Frommer ve ark., 1992).
-Metillenmemiş sitozinler bisülfit tedavisi ile urasile dönüşür, metillenmiş sitozinler ise değişmez (Clark ve ark., 1994).
-Tek baz çözünürlüğünde metilasyon profillemesi sağlar (Cokus ve ark., 2008; Lister ve ark., 2008).
-Whole-genome bisulfite sequencing (WGBS) tüm genomdaki CpG, CHG ve CHH metilasyon paternlerini ortaya çıkarır (Lister ve ark., 2008; Zemach ve ark., 2010).
ATAC-seq (Assay for Transposase-Accessible Chromatin using Sequencing):
-Açık kromatin bölgelerini (transkripsiyon faktörlerinin bağlanabileceği bölgeler) tanımlar (Buenrostro ve ark., 2013).
-Tn5 transpozazının tercihli olarak açık kromatin bölgelerine entegre olması prensibine dayanır (Buenrostro ve ark., 2015).
-Düzenleyici elementlerin (enhancers, promoters) tanımlanmasında kullanılır (Lu ve ark., 2017; Bajic ve ark., 2018).
Hi-C ve Kromatin Konformasyon Analizi:
-Üç boyutlu kromatin organizasyonunu ve uzun menzil DNA etkileşimlerini ortaya çıkarır (Lieberman-Aiden ve ark., 2009).
-Topologically associating domains (TAD) ve kromatin loop yapılarını tanımlar (Dixon ve ark., 2012; Nora ve ark., 2012).
-Enhancer-promoter etkileşimlerinin haritalanmasında önemli bilgiler sağlar (Feng ve ark., 2014; Liu ve ark., 2016).
2.3Bitkilerde Epigenetik Mühendisliği: Güncel Araştırmalar ve Uygulamalar
2.3.1 CRISPR tabanlı epigenom düzenleme
CRISPR-Cas9 sisteminin genetik düzenleme alanında devrim yaratmasının ardından, bu sistem epigenom düzenlemesi için de adapte edilmiştir (Pulecio ve ark., 2017). Katalitik olarak inaktif Cas9 (dCas9), DNA kesme aktivitesini kaybetmiş ancak DNA'ya sekans-spesifik bağlanma yeteneğini korumuş bir varyantıdır (Qi ve ark., 2013). dCas9, epigenetik efektör proteinleriyle füzyone edilerek, hedef genomik lokalizasyonlarda epigenetik modifikasyonlar gerçekleştirilebilir (Thakore ve ark., 2016):
dCas9-DNMT Füzyonları:
-dCas9 ile DNA metiltransferaz domainlerinin (örneğin DNMT3A) füzyone edilmesi, seçilen genlerin promotör bölgelerinde metilasyon indüksiyonu sağlar (Vojta ve ark., 2016).
-Zhao ve arkadaşları (2016), dCas9-DNMT3A sistemiyle Arabidopsis'te hedef genleri sessizleştirmiştir.
-Bitki çalışmalarında, dCas9-DRM füzyonları ve RdDM mekanizmasının birleştirilmesi üzerine araştırmalar devam etmektedir (Gallego-Bartolomé, 2020; Papikian ve ark., 2019).
dCas9-TET/ROS Füzyonları:
-DNA demetilasyon domenlerinin (örneğin TET enzimlerinin katalitik domainleri veya bitkilerde ROS1) dCas9'a füzyone edilmesi, spesifik bölgelerde demetilasyon sağlar (Gallego-Bartolomé ve ark., 2018; Maeder ve ark., 2013).
-Bu yaklaşım, susturulmuş genlerin yeniden aktivasyonu için kullanılabilir (Liu ve ark., 2018).
dCas9-HAT/HDAC Füzyonları:
-Histon asetiltransferaz (HAT) veya histon deasetilaz (HDAC) domainlerinin dCas9'a bağlanması, hedef kromatin bölgelerinde asetilasyon seviyelerini kontrol eder (Kwon ve ark., 2017).
-Hilton ve arkadaşları (2015), dCas9-p300 (HAT) sistemiyle memeli hücrelerinde hedef genleri aktive etmiştir.
-Bitkilerde benzer yaklaşımlar, stres yanıt genlerinin ifadesini modüle etmek için geliştirilmektedir (Roca Paixão ve ark., 2019).
Çoklu Epigenom Düzenleme:
-Aynı anda birden fazla epigenetik modifikasyonun gerçekleştirilmesi (örneğin DNA metilasyonu ve histon modifikasyonlarının kombinasyonu) daha güçlü ve kararlı gen ifade değişiklikleri sağlar (Amabile ve ark., 2016).
-Multipleks gRNA sistemleri, birden fazla genomik bölgenin eş zamanlı düzenlenmesini mümkün kılar (McCarty ve ark., 2020).
2.3.2 Epigenetik düzenleyici kimyasallar
Küçük molekül epigenetik düzenleyiciler (epi-drugs), DNA metilasyonunu veya histon modifikasyonlarını hedefleyerek gen ekspresyonunu değiştirir (Jones ve ark., 2016; Arrowsmith ve ark., 2012):
DNMT İnhibitörleri:
-5-azasitidin (5-azaC) ve 5-aza-2'-deoksisitidin (Desitabin): Sitozin analoglarıdır ve DNA'ya entegre olduklarında DNMT enzimlerini kovalent olarak bağlayarak inhibe ederler (Christman, 2002). FDA onaylı kanser ilaçlarıdır (Kaminskas ve ark., 2005) ancak bitki uygulamalarında da kullanılmıştır (Baubec ve ark., 2009; Fieldes ve ark., 2005).
- Zebularin: Daha stabil bir sitozin analoğudur ve oral biyoyararlanımı daha iyidir (Yoo ve ark., 2008; Cheng ve ark., 2004).
Bitki çalışmalarında, 5-azaC uygulamasının kuraklık ve tuz stresine toleransı artırdığı gösterilmiştir (Wang ve ark., 2011; Zhong ve ark., 2010). Ancak genom geneli demetilasyon, hedef dışı etkilere yol açabilir ve bu nedenle doz optimizasyonu kritiktir (Gowher ve Jeltsch, 2004).
HDAC İnhibitörleri:
-Trikostatin A (TSA): Klasik HDAC inhibitörüdür (Yoshida ve ark., 1990). Nanomolar konsantrasyonlarda etkilidir ve histon hiperasetilasyonuna yol açar (Chen ve ark., 2010).
- Sodyum Bütirat: Daha az potent ancak daha güvenli bir HDAC inhibitörüdür (Candido ve ark., 1978). Bitki hücre kültürlerinde yaygın olarak kullanılır (Tanaka ve ark., 2008).
-Valproik Asit (VPA): Klinik kullanımı olan bir HDAC inhibitörüdür (Göttlicher ve ark., 2001; Phiel ve ark., 2001).
HDAC inhibitörleri, stres yanıt genlerinin kromatin yapısını açarak daha hızlı transkripsiyona izin verir (Sako ve ark., 2016; Ueda ve ark., 2017). Ancak, geniş spektrumlu HDAC inhibisyonu global gen ekspresyon değişikliklerine neden olabilir (Johnsson ve ark., 2013).
HAT Aktivatörleri:
- Histon asetilasyon aktivitesini artıran küçük moleküller daha az gelişmiş durumdadır (Dekker ve Haisma, 2009).
- Pentamidin gibi moleküllerin p300 HAT aktivitesini artırdığı gösterilmiştir (Sbardella ve ark., 2008).
HMT ve HDM Modülatörleri:
- Histon metiltransferaz (HMT) ve histon demetilaz (HDM) inhibitörleri, spesifik histon metilasyon paternlerini değiştirmek için kullanılabilir (Kruidenier ve ark., 2012; Konze ve ark., 2013).
- UNC1999 (EZH2 inhibitörü) H3K27me3 seviyelerini azaltır (Konze ve ark., 2013).
-GSK-J4 (JMJD3 inhibitörü) H3K27me3 seviyelerini artırır (Kruidenier ve ark., 2012; Heinemann ve ark., 2014).
2.3.3Nanoteknoloji ve epigenetik ilaç taşıma sistemleri
Epigenetik düzenleyici moleküllerin bitkilere etkin ve hedefli iletimi, nanoteknoloji ile mümkün hale gelmiştir (Wang ve ark., 2016). Nanopartiküller, koruma, kontrollü salınım ve hücresel hedefleme avantajları sunar (Cunningham ve ark., 2018).
Lipit Bazlı Nanopartiküller:
- Lipozomlar ve katı lipit nanopartiküller (SLN), hidrofilik ve hidrofobik molekülleri kapsülleyebilir (Karny ve ark., 2018; Torchilin, 2005).
- Bitki hücrelerinin plazma membranıyla füzyon yaparak içeriği sitoplazmaya aktarır (Demirer ve ark., 2019).
- PEDAS sisteminde kullanılan nano-lipit kompleksler bu kategoriye girer (Mitter ve ark., 2017).
Polimer Nanopartiküller:
- Kitosan, PLGA (Poli Laktik-ko-Glikolik Asit) ve PEI (Polietilenimin) bazlı nanopartiküller, nükleik asit ve protein taşımacılığında yaygın kullanılır (Nair ve ark., 2010; Zhang ve ark., 2021).
-Pozitif yüklü polimerik nanopartiküller, negatif yüklü hücre membranlarıyla elektrostatik etkileşim yoluyla hücre içine alınır (Wang ve ark., 2018).
Karbon Nanomateryaller:
- Grafen oksit ve karbon nanotüpler, yüksek yüzey alanı ve benzersiz optik özellikleri nedeniyle ilgi çekmektedir (Begum ve ark., 2011; Hu ve ark., 2014).
- DNA, RNA ve protein yükleri taşıyabilir (Demirer ve ark., 2020).
- Fitotoksisite endişeleri, dikkatli doz optimizasyonu gerektirmektedir (Mukherjee ve ark., 2016).
Mezogözenekli Silika Nanopartiküller:
- Kontrollü gözenek boyutu ve yüksek yükleme kapasitesi sunar (Torney ve ark., 2007; Sun ve ark., 2018).
- pH veya enzim duyarlı kapaklarla donatılarak, hedef doku veya organelde salınım sağlanabilir (Yang ve ark., 2016).
Peptid Tabanlı Hücre Penetrasyonu Artırıcı Ajanlar (CPP):
- TAT peptid (HIV-1 Trans-Aktivatörü) gibi hücre penetrasyonu artırıcı peptidler, kargonun hücre membranından geçişini kolaylaştırır (Chang ve ark., 2005; Eggenberger ve ark., 2010).
-Bitki hücrelerinde kullanımı sınırlıdır ancak protoplast uygulamalarında etkilidir (Chugh ve ark., 2010).
2.4Mikrobiyom ve Bitki-Mikrop Etkileşimleri
2.4.1 Rizosfer mikrobiyomunun kompozisyonu
Rizosfer, bitki kökleri ve çevrelerindeki toprak arasındaki dar ara yüz bölgesidir ve zengin mikrobiyal aktivite gösterir (Hiltner, 1904; Philippot ve ark., 2013). Kök eksudatları (şekerler, amino asitler, organik asitler, sekonder metabolitler), mikrobiyal toplulukları şekillendirir (Bais ve ark., 2006; Badri ve Vivanco, 2009).
Faydalı Mikroorganizma Grupları:
1.Azot Fikse Eden Bakteriler:
- Rhizobia: Leguminlerle simbiyotik ilişki kurar ve kök nodüllerinde atmosferik azotu amonyağa dönüştürür (Oldroyd, 2013; Gage, 2004).
-Azospirillum, Azotobacter: Serbest yaşayan azot fikse eden bakterilerdir ve birçok mahsulde bitki büyümesini teşvik eder (Steenhoudt ve Vanderleyden, 2000; Vessey, 2003).
2.Fosfat Çözen Bakteriler:
- Bacillus, Pseudomonas: Organik fosfor bileşiklerini mineralize ederek bitkinin kullanabileceği formlara dönüştürür (Richardson ve Simpson, 2011; Sharma ve ark., 2013).
-Organik asit (glukonik asit, sitrik asit) salgılayarak, çözünmeyen fosfat kaynaklarını mobilize eder (Rodríguez ve Fraga, 1999).
3.Mikorizal Funguslar:
- Arbüsküler Mikorizal Funguslar (AMF): Bitki köklerine penetrasyon yaparak arbüsküller oluşturur ve besin elementi (özellikle fosfor) alımını artırır (Smith ve Read, 2008; Parniske, 2008).
- Kuraklık ve tuz stresine toleransı artırır (Augé, 2001; Ruiz-Lozano ve ark., 2012).
-Toprak agrega yönünü iyileştirir (Rillig ve Mummey, 2006).
4.Bitki Büyüme Teşvik Eden Rizobakteriler (PGPR):
-Bacillus subtilis, Pseudomonas fluorescens: Fitohormon üretimi (IAA, gibberellinler), siderofor salınımı ve biyokontrol özellikleri ile bilinirler (Lugtenberg ve Kamilova, 2009; Compant ve ark., 2005).
-Sistemik direnci indükleyerek (ISR: Induced Systemic Resistance) patojen toleransını artırır (Pieterse ve ark., 2014; Van Loon, 2007).
2.4.2 Mikrobiyom-epigenetik etkileşimleri
Mikrobiyal topluluklar, bitkilerin epigenetik durumunu etkileyebilir ve bu etki "mikrobiyom-epigenom çapraz konuşması" (microbiome-epigenome crosstalk) olarak adlandırılır (Berendsen ve ark., 2012; Thiebaut ve ark., 2019):
Mikrobiyal Metabolitler ve Epigenezim Modülasyon:
-Bütirat: Bakteriyel fermentasyonun bir ürünüdür ve bilinen bir HDAC inhibitörüdür (Waldecker ve ark., 2008). Bitki dokularında histon asetilasyonunu artırabileceğine dair kanıtlar bulunmaktadır (Lämke ve Bäurle, 2017).
- Poliaminler (Spermidin, Spermin): Bazı rizobakteriler tarafından üretilir (Kuznetsov ve ark., 2006) ve kromatin yapısını etkileyerek gen ekspresyonunu modüle edebilir (Tiburcio ve ark., 2014).
Mikrobiyal Sinyal Molekülleri:
- Quorum Sensing Molekülleri (AHL - Açil-Homoserin Laktonlar): Bakteriyel iletişim molekülleridir ve bitki gen ekspresyonunu modüle edebilir (Mathesius ve ark., 2003; Schikora ve ark., 2011). AHL'lerin bitkilerde savunma yanıtlarını ve kök gelişimini etkilediği gösterilmiştir (Ortiz-Castro ve ark., 2008).
- Lipopolisakkaritler (LPS): Gram-negatif bakterilerin hücre duvarı bileşenidir ve bitki immun yanıtlarını tetikler (Newman ve ark., 2013). Bu süreç, kromatin yeniden yapılanması ve epigenetik değişiklikler içerir (Ma ve ark., 2021).
Mikorizal Enfeksiyon ve Epigenetik:
- Arbüsküler mikorizal fungus (AMF) enfeksiyonu sırasında, bitki köklerinde DNA metilasyon paternlerinde değişiklikler gözlenir (Vangelisti ve ark., 2020; Cicatelli ve ark., 2014).
-Simbiyoz oluşumu için gerekli genlerin (örneğin SYMRK, CASTOR, POLLUX) düzenlenmesi epigenetik mekanizmalarla kontrol edilir (Oldroyd, 2013; Satgé ve ark., 2016).
2.5Mevcut Ticari Uygulamalar ve Sınırlamalar
2.5.1 Biyostimülantlar ve biyopestisitler
Biyostimülantlar, bitki büyümesini ve stres toleransını artıran maddelerdir (besleyici özellikler taşımayan; du Jardin, 2015). Mevcut biyostimülant pazarı 2023 yılında 3.2 milyar dolara ulaşmıştır ve 2030'da 6.8 milyar dolara çıkması beklenmektedir
Mevcut Biyostimülant Kategorileri:
- Humik ve fulvik asitler (Canellas ve ark., 2015)
- Protein hidrolizatları ve amino asitler (Colla ve ark., 2015)
- Deniz yosunu ekstraktları (Battacharyya ve ark., 2015)
- Faydalı mikroorganizmalar (Vessey, 2003)
- Kitosan ve diğer biyopolimerler (Pichyangkura ve Chadchawan, 2015)
Sınırlamalar:
- Etkinlik değişkenliği: Çevresel koşullara, mahsul tipine ve uygulama zamanlamasına göre büyük farklılıklar gösterir (Yakhin ve ark., 2017).
- Standardizasyon eksikliği: Birçok ürün karmaşık karışımlardır ve aktif bileşenler tam olarak karakterize edilmemiştir (Ricci ve ark., 2019).
-Etki mekanizması belirsizliği: Çoğu biyostimülantın moleküler etki mekanizması tam anlaşılmamıştır (Brown ve Saa, 2015).
2.5.2 RNAi bazlı biyopestisitler
RNAi teknolojisi, spesifik zararlı organizmaların hedef genlerini susturarak biyokontrol sağlar (Fire ve ark., 1998; Baum ve ark., 2007). İlk ticari RNAi ürünü 2017'de piyasaya çıkmıştır (DvSnf7 dsRNA, Batı kök kurdu'na karşı; Bachman ve ark., 2013; Head ve ark., 2017).
Avantajlar:
- Yüksek spesifiklik: Hedef dışı organizmalara minimal etki yapar(Whyard ve ark., 2009).
- Çevre dostu: Hızla parçalanır ve biyobirikim göstermez (Auer ve Frederick, 2009).
- Direnç gelişimine karşı daha az yatkındır (Zotti ve Smagghe, 2015).
Zorluklar:
- Yüksek üretim maliyeti: dsRNA sentezi pahalıdır (Taning ve ark., 2020).
- Stabilite sorunları: dsRNA molekülleri çevresel RNazlar tarafından hızla degrade edilir (Dubelman ve ark., 2014).
- Bitki yüzeyine yapışma ve hücre içi alım: Kutikula ve hücre duvarı bariyerleri etkinliği sınırlar (Wang ve Jin, 2017).
PEDAS sistemi, VLP tabanlı kapsülasyon ile bu stabilite ve alım sorunlarını çözmeyi hedeflemektedir (Mitter ve ark., 2017; Demirer ve ark., 2019).
2.6PEDAS Sisteminin Literatürdeki Konumu
Mevcut araştırmalar, epigenetik düzenleme, RNAi ve mikrobiyom mühendisliğini genellikle ayrı alanlarda ele almaktadır. PEDAS sistemi, bu üç yaklaşımı entegre eden ve yapay zeka destekli otomasyonla birleştiren yenilikçi bir platformdur. Literatürde, benzer kapsamlı entegre sistemlere rastlanmamaktadır.
PEDAS'ın Yenilikçi Yönleri:
1.Çoklu Stres Hedefleme: Tek bir platform üzerinden abiyotik ve biyotik streslere karşı eş zamanlı müdahale imkanı sunar. Bitkilerde farklı stres türlerinin etkileşimi karmaşık olup (Atkinson ve Urwin, 2012), PEDAS bu karmaşıklığa bütüncül bir çözüm getirmeyi hedeflemektedir.
2.GDO-Dışı Yaklaşım: Transgenik modifikasyon gerektirmeyen, mevcut regülasyonlara uyumlu bir teknolojidir (Sprink ve ark., 2016). Epigenetik mühendisliği, kalıcı genetik değişiklikler yapmadan gen ifadesini modüle ederek düzenleyici avantajlar sunar (Papikian ve ark., 2019).Satır Aralıkları
3.Geri Dönüşlülük: Epigenetik modifikasyonların geçici doğası, uzun vadeli ekolojik riskleri minimize eder (Bruce ve ark., 2007). Stres ortadan kalktığında bitkinin orijinal epigenetik durumuna dönebilmesi, güvenlik açısından kritik bir özelliktir (Lämke ve Bäurle, 2017).
4.IoT ve Yapay Zeka Entegrasyonu: Gerçek zamanlı izleme ve otomatik doz ayarlama ile hassas tarım uygulamalarını mümkün kılar (Wolfert ve ark., 2017). Yapay zeka, bitki ihtiyaçlarını öngörerek kaynak kullanımını optimize eder (Kamilaris ve Prenafeta-Boldú, 2018).
5.Mikrobiyom Sinerji: Epigenetik programlama ile faydalı mikrobiyom inokulasyonunun kombinasyonu, sinerjistik etkiler yaratır (Pieterse ve ark., 2014). Mikrobiyal toplulukların bitki epigenomunu şekillendirme potansiyeli, bu sinerjinin temelini oluşturur (Thiebaut ve ark., 2019).
Bu özellikler, PEDAS'ı mevcut biyoteknolojik yaklaşımlardan farklılaştırmakta ve sürdürülebilir tarım için yeni bir paradigma sunmaktadır.
3.PEDAS EPİGENETİK PROGRAMLAMA MODÜLÜ
3.1Sistem Mimarisi ve Genel Tasarım
PEDAS epigenetik modülü, siber-fiziksel tarım sistemleri yaklaşımına dayanan üç katmanlı bir mimari kullanır. PEDAS sisteminin epigenetik programlama modülü, bitkilerin stres yanıt kapasitesini proaktif olarak optimize etmek üzere tasarlanmıştır (Bruce ve ark., 2007; Gallego-Bartolomé, 2020). Sistem, üç temel katmandan oluşur:
3.1.1Algılama katmanı (sensör ağı)
Algılama katmanı, tarla koşullarını gerçek zamanlı olarak izleyen IoT sensör ağından oluşur (Wolfert ve ark., 2017; Talavera ve ark., 2017):
Toprak Sensörleri:
- Toprak Nem Sensörleri: Kapasitif veya TDR (Time Domain Reflectometry) tabanlı sensörler, kök bölgesindeki nem içeriğini ölçer (Robinson ve ark., 2008). 15 cm, 30 cm ve 60 cm derinliklerde yerleştirilen sensörler, kök su alım profilini haritalandırır (Vereecken ve ark., 2008).
- Toprak EC (Elektriksel İletkenlik) Sensörleri: Tuzluluk seviyesini tahmin eder (Corwin ve Lesch, 2005). 0-7 dS/m aralığında hassas ölçüm yapar (Rhoades ve ark., 1999).
- pH Sensörleri: Toprak reaksiyonunu izler (4.0-9.0 aralığı; Schofield ve Taylor, 1955).
-Sıcaklık Sensörleri: Toprak sıcaklığını ölçer; kök bölgesi termal stresi için kritiktir. (Bristow, 1998).
Mikroklima Sensörleri:
-Hava Sıcaklığı ve Nem: DHT22 veya daha hassas SHT31 sensörleri kullanılır (Dunn ve ark. 2015)
-Yaprak Islaklık Sensörleri: Fungal hastalık riskini tahmin etmek için kullanılır (Huber ve Gillespie, 1992; Sentelhas ve ark., 2004).
-PAR (Photosynthetically Active Radiation) Sensörleri: Fotosentetik aktiviteyi etkileyen ışık yoğunluğunu ölçer (McCree, 1972).
-Vapor Pressure Deficit (VPD) Hesaplama Modülü:
-Hava sıcaklığı ve bağıl nem verilerinden türetilir ve bitki su stresinin güçlü bir göstergesidir.
Bitki Bazlı Sensörler:
- Dendrometreler: Gövde çapındaki günlük değişimleri ölçerek su stresini tespit eder (Fernández ve Cuevas, 2010; Drew ve ark., 2008).
-Klorofil Floresans Sensörleri: Fotosentetik etkinliği ve stres göstergelerini (Fv/Fm oranı) izler (Maxwell ve Johnson, 2000; Baker, 2008).
- Hiperspektral Kameralar (Drone bazlı): Bitki sağlığı indeksleri (NDVI, PRI, WBI) hesaplar (Zarco-Tejada ve ark., 2012; Gamon ve ark., 1992).
Veri İletişimi:
- LoRaWAN veya NB-IoT teknolojileri kullanılarak düşük güç tüketimiyle uzun menzilli veri iletimi sağlanır (Sinha ve ark., 2017; Mekki ve ark., 2019).
-Edge computing kapasitesi ile bazı ön-işlemeler sensör nodlarında gerçekleştirilir (Satyanarayanan, 2017).
3.1.2İşlem katmanı (veri analizi ve karar verme)
Toplanan veriler, bulut tabanlı veya yerel sunucularda analiz edilir (Kamilaris ve Prenafeta-Boldú, 2018):
Makine Öğrenmesi Modelleri:
- Stres Tahmini Modelleri: Geçmiş veriler ve hava durumu tahminleri kullanılarak, 3-7 gün öncesinden stres olayları öngörülür (van Klompenburg ve ark., 2020).
- Random Forest, Gradient Boosting ve LSTM (Long Short-Term Memory) ağları kullanılır (Breiman, 2001; Hochreiter ve Schmidhuber, 1997; Friedman, 2001).
- Model girişleri: meteorolojik veriler, toprak parametreleri, fenolojik aşama, geçmiş stres olayları (Chlingaryan ve ark., 2018).
-Model çıkışı: stres olasılığı (0-1 skala) ve şiddeti tahmini.
-Doz Optimizasyon Algoritmaları: Epigenetik modülatörlerin optimal konsantrasyonlarını belirler (Shahrayini ve ark., 2021).
-Bayesian optimization yaklaşımı ile parametre uzayı taranır (Snoek ve ark., 2012).
-Çoklu objektif optimizasyonu: verim maksimizasyonu, maliyet minimizasyonu, çevre etkisi minimizasyonu (Deb ve ark., 2002).
Bilgi Sistemleri Entegrasyonu:
-Mahsul yönetim sistemleri (FMIS: Farm Management Information Systems) ile entegrasyon (Sørensen ve ark., 2010).
-Tarihsel verim ve yönetim verilerinin analizi (Fountas ve ark., 2006).
-Ekonomik analiz modülleri: girdi-çıktı analizi, ROI hesaplamaları (Griffin ve ark., 2018).
3.1.3Uygulama katmanı (nano-formülasyon iletimi)
Epigenetik modülatörler, nano-lipit kompleksler içerisinde bitkilere uygulanır (Wang ve ark., 2016; Demirer ve ark., 2019):
Uygulama Yöntemleri:
- Kök Bölgesi Enjeksiyonu: Damla sulama sistemine entegre edilmiş dozaj ünitesi ile, nano-formülasyon doğrudan kök bölgesine iletilir (Karny ve ark., 2018).
- Yaprak Püskürtme: Stomatik absorpsiyon için surfaktan içeren formülasyonlar kullanılır (Eichert ve Goldbach, 2008; Fernandez ve Eichert, 2009).
-Tohum Kaplama (Seed Priming): Çimlenme öncesi epigenetik ön-programlama (Paparella ve ark., 2015; Wojtyla ve ark., 2016).
Otomatik Dozaj Kontrol Ünitesi:
- Peristaltik pompalar ile hassas doz kontrolü (±2% hata payı; Ulusoy ve ark., 2016).
- pH ve EC ayarlama: formülasyonun stabilitesini ve bitki alımını optimize eder (Tadros, 2013).
-QR kod veya RFID tabanlı takip: hangi parselin, hangi tarihte, ne kadarlık uygulama aldığı kaydedilir (Ruiz-Garcia ve ark., 2009).
3.2Hedef Gen Grupları ve Epigenetik Stratejiler
PEDAS sistemi, farklı stres tiplerini hedefleyen gen modüllerini kontrol eder (Atkinson ve Urwin, 2012). Her stres tipi için optimize edilmiş epigenetik müdahale stratejileri geliştirilmiştir.
3.2.1Kuraklık ve osmotik stres modülü
Hedef Genler:
1.NCED3 (9-cis-Epoxycarotenoid Dioxygenase 3):
- ABA biyosentezinde anahtar enzimdir (Iuchi ve ark., 2001; Tan ve ark., 2003).
- Kuraklık stresi altında hızla indüklenir.
- Epigenetik Strateji: NCED3 promotöründe H3K4me3 zenginleştirmesi ve DNA demetilasyonu (Kim ve ark., 2008; Ding ve ark., 2012). Bu modifikasyonlar, gen transkripsiyonunu “hazır” durumda tutar.
2.PIP1 ve PIP2 (Plasma membrane Intrinsic Proteins):
- Aquaporin ailesine ait proteinlerdir ve su transportunu düzenler (Maurel ve ark., 2008; Chaumont ve Tyerman, 2014).
-Kök ve yaprak dokularında eksprese edilir.
- Epigenetik Strateji: PIP genlerinin promotör bölgelerinde H3K9ac artışı (Sade ve ark., 2018). HDAC inhibitörleri (TSA, 0.1-0.5 µM) uygulanarak kromatin erişilebilirliği artırılır (Chen ve ark., 2010).
3.RD22 ve RD29A (Responsive to Desiccation):
- Dehidrin ve LEA protein ailelerinden üyelerdir (Yamaguchi-Shinozaki ve Shinozaki, 1993; Close, 1996).
- Hücresel su homeostazını korur.
- Epigenetik Strateji: CpG adalarında DNA demetilasyonu (5-azaC, 0.5-2 µM; Wang ve ark., 2011). Kromatin yeniden şekillendirme kompleksleri (SWI/SNF) aktivasyonu (Han ve ark., 2015).
Beklenen Moleküler Değişiklikler:
- ABA içeriğinde 2-3 kat artış (48 saat içinde; Iuchi ve ark., 2001).
- Stoma iletkenliğinde %30-40 azalma (Miyashita ve ark., 2005).
-Kök hidrolik iletkenlikte %20-30 artış (Maurel ve ark., 2008).
- Prolin ve çözünür şeker birikiminde %50-100 artış (Szabados ve Savouré, 2010).
Fizyolojik Sonuçlar:
- Yaprak su potansiyelinde daha az düşüş (-1.5 MPa yerine -1.0 MPa; Hsiao, 1973).
- Fotosentetik etkinlikte daha az kayıp (Fv/Fm oranı 0.75 üzerinde kalır; Maxwell ve Johnson, 2000).
-Biyomas üretiminde %20-30 artış (kuraklık koşullarında; Passioura, 2007).
3.2.2. Tuzluluk toleransı modülü
Hedef Genler:
1.SOS1 (Salt Overly Sensitive 1):
- Na⁺/H⁺ antiporteridir; plazma membranında Na⁺ ekskresyonunu sağlar (Shi ve ark., 2000; Qiu ve ark., 2002).
- Tuz stresine adaptasyonda kritik rol oynar.
- Epigenetik Strateji: SOS1 promotöründe H3K4me3 ve H3K9ac artışı (Sako ve ark., 2016). DNA demetilasyonu ile gen ekspresyonunun konstitutif olarak yüksek tutulması (Yaish ve ark., 2018).
2.NHX1 (Na⁺/H⁺ Exchanger 1):
- Vakuolar membran antiporteridir; Na⁺’nın vakuol içinde sekestre edilmesini sağlar (Apse ve ark., 1999; Gaxiola ve ark., 1999).
- Epigenetik Strateji: Promotör bölgede metilasyonun uzaklaştırılması ve histon asetilasyonunun artırılması (Sokol ve ark., 2007).
3.HKT1 (High-affinity K⁺ Transporter 1):
- Ksilemde Na⁺ geri alımını sağlar ve yapraklara Na⁺ taşınmasını sınırlar (Mäser ve ark., 2002; Horie ve ark., 2009).
- Epigenetik Strateji: Kromatin açıklığının artırılması, SWI/SNF kompleks aktivasyonu (Baetz ve Martinoia, 2014).
Beklenen Moleküler Değişiklikler:
-Yaprak Na⁺ içeriğinde %40-50 azalma (Munns ve Tester, 2008).
- K⁺/Na⁺ oranında %60-80 artış (Maathuis ve Amtmann, 1999).
- Uyumlu çözünür madde (glisin betain, prolin) birikiminde artış (Flowers ve Colmer, 2008).
Fizyolojik Sonuçlar:
- 100-150 mM NaCl konsantrasyonunda normal büyümenin %70-80’inin sürdürülmesi (Munns, 2002).
- Klorozis ve nekroz semptomlarında gecikme (Tester ve Davenport, 2003).
- Verim kaybının %15-20’ye indirilmesi (kontrolde %50-60 kayıp; Flowers ve ark., 2010).
3.2.3. Soğuk toleransı modülü
Hedef Genler:
1.CBF/DREB1 Genler (C-repeat Binding Factors):
-Ana soğuk yanıt transkripsiyon faktörleridir.
-ICE1 tarafından düzenlenir.
-Epigenetik Strateji: CBF promotörlerinde H3K4me3 artışı ve H3K27me3 azaltılması (EZH2 inhibitörü UNC1999 kullanılarak).
2.COR Genler (Cold Regulated):
-CBF hedef genleridir; antifreeze proteinler, chaperonlar ve membran stabilizan proteinleri kodlar.
-Epigenetik Strateji: Kromatin erişilebilirliğinin artırılması, DNA demetilasyonu.
3.FAD Genler (Fatty Acid Desaturases):
-Membran lipid desaturasyonunu katalize eder; membran fluiditesini düşük sıcaklıklarda korur.
-Epigenetik Strateji: Promotör asetilasyonunun artırılması.
Beklenen Moleküler Değişiklikler:
-Çoklu doymamış yağ asitlerinde (PUFA) %30-40 artış.
-Çözünür şeker içeriğinde artış (osmotik ayarlama).
-Antifreeze protein ekspresyonunda 5-10 kat artış.
Fizyolojik Sonuçlar:
-Donma toleransının -5°C’den -8°C’ye genişletilmesi.
-Elektrolit sızıntısında %40-50 azalma.
-Soğuk şoku sonrası iyileşme süresinin %30-40 kısalması.
3.2.4 Patojen direnci modülü
Hedef Genler:
1.NPR1 (Nonexpressor of Pathogenesis-Related genes 1):
-SAR’ın ana düzenleyicisidir.
-SA sinyalleme ile aktivasyon.
-Epigenetik Strateji: NPR1 ve hedef PR genlerinde H3K4me3 zenginleştirmesi, kromatin açıklığı artışı.
2.PR Genler (Pathogenesis-Related):
-PR1, PR2, PR5 gibi proteinler antimikrobiyal aktivite gösterir.
-Epigenetik Strateji: Promotör bölgelerinde histon asetilasyonu artışı, DNA demetilasyonu.
3.PDF1.2 (Plant Defensin 1.2):
-JA/ET yanıtının markeridir; nekrotrofik patojenlere karşı etkili.
-Epigenetik Strateji: Kromatin erişilebilirliğinin optimize edilmesi.
RNAi Entegrasyonu:
-Patojen spesifik siRNA’lar VLP içinde taşınarak hedef patojen genlerini susturur (detaylar Bölüm 4’te).
Beklenen Sonuçlar:
-Hastalık insidens oranında %50-70 azalma.
-Lezyonların gelişim hızında yavaşlama.
-Sistemik savunma yanıtlarının 24-48 saat erkene alınması.
3.3Nano-Lipit Formülasyon Teknolojisi
3.3.1Formülasyon bileşimi
PEDAS epigenetik modülatör formülasyonu, aşağıdaki bileşenlerden oluşur:
Lipit Taşıyıcı Sistem:
-DOPC (1,2-Dioleoyl-sn-glycero-3-phosphocholine): Ana fosfolipit bileşeni. Lipozom oluşumunda merkezi rol.
-Kolesterol: Membran stabilitesini artırır ve lipit ikili tabakasını düzenler (lipit:kolesterol 2:1 oranı).
-PEG-Lipid (Polyethylene Glycol Conjugated Lipid): Nanopartikül stabilitesini artırır, agregasyonu önler ve “stealth” özellik kazandırır.
Epigenetik Modülatörler:
-5-azacytidine (5-azaC): 0.5-2 µM konsantrasyonda, DNA demetilasyonu için.
-Trichostatin A (TSA): 0.1-0.5 µM konsantrasyonda, HDAC inhibisyonu için.
-S-Adenosylhomocysteine (SAH): Doğal DNMT inhibitörü, 1-5 µM.
-UNC1999: Seçici EZH2 inhibitörü, H3K27me3 seviyelerini azaltmak için, 0.5-1 µM (sadece soğuk toleransı modülünde).
Penetrasyon Artırıcılar:
-Sürfaktanlar: Tween 80 veya Triton X-100 (%0.01-0.05), stoma ve kütikula penetrasyonunu artırır.
-Dimetil Sülfoksit (DMSO): %1-2 konsantrasyonda, hücre membran geçirgenliğini artırır.
Stabilizatörler ve pH Tamponu:
-HEPES buffer: pH 7.0-7.4 aralığında stabilite sağlar.
-EDTA: Metal kelatörüdür, formülasyon stabilitesini korur, 0.1-0.5 mM.
3.3.2Nanopartiküllerin hazırlanması
Thin-Film Hydration Yöntemi:
1.Lipitler (DOPC, kolesterol, PEG-lipid) kloroform-metanol karışımında (2:1 v/v) çözülür.
2.Döner buharlaştırıcıda (rotary evaporator) organik çözücüler uzaklaştırılır ve ince lipid filmi oluşturulur.
3.Film, epigenetik modülatörler içeren sulu faz ile rehidrate edilir (65°C, 1 saat).
4.Elde edilen multilamellar veziküller, sonikasyon veya ekstrüzyon ile unilamellar vezikülere (lipozomlar) dönüştürülür.
Ekstrüzyon:
-Polikarbonat membranlardan (20–50 nm gözenek boyutu) 10-15 geçiş yapılarak homojen boyut dağılımı sağlanır.
Karakterizasyon:
-Partikül boyutu: Dinamik ışık saçılımı (DLS) ile ölçülür. Hedef: 20–50 nm.
-Zeta potansiyali: Elektroforetik ışık saçılımı ile ölçülür. Negatif zeta potansiyeli (-20 mV ile -40 mV) stabiliteyi gösterir.
-Enkapsülasyon verimliliği: HPLC veya UV-Vis spektrofotometre ile belirlenir.
Hedef: >80%.
-Morfoloji: Transmisyon elektron mikroskobu (TEM) ile görselleştirilir.
3.3.3Bitki hücresine alım mekanizmaları
Nano-lipit kompleksler bitki hücrelerine çeşitli mekanizmalarla alınır:
Endositozis:
-Klathrin aracılı endositozis: Reseptör-ligand etkileşimleri üzerinden.
Membran Füzyonu:
-Lipozomlar, plazma membranı ile doğrudan füzyon yaparak içeriklerini sitoplazmaya aktarabilir.
Makropinositoz:
-Büyük hücre membran invaginasyonları ile sıvı faz endositozisi.
Kök Hücre Duvarı Penetrasyonu:
-Kök uç bölgelerinde hücre duvarı daha incedir ve penetrasyon daha kolaydır.
-Yaralanma bölgeleri ve lateral kök çıkış noktaları, preferansiyel giriş noktalarıdır.
3.3.4Kontrollü Salınım ve Hedefleme
pH Duyarlı Salınım:
-Lipozomlar, farklı hücresel kompartmanlardaki pH değişikliklerine (örneğin, endozomlarda asidik pH) duyarlı olacak şekilde tasarlanabilir.
-pH düşüklüğünde lipozomal membran destabilize olur ve içerik salınır.
Doku Spesifik Hedefleme:
-Peptid ligandları (örneğin, kök spesifik reseptörleri hedefleyen peptidler) lipozom yüzeyine konjuge edilebilir.
-Manyetik nanopartiküller eklenerek, eksternal manyetik alan ile hedefleme yapılabilir (deneysel aşamada).
3.4Uygulama Metodolojisi ve Zaman Profili
3.4.1Uygulama protokolü
Zamanlama:
Epigenetik programlama, bitkilerin kritik fenolojik aşamalarında veya öngörülen stres olaylarından 3-7 gün önce uygulanır.
Fide Dönemi Uygulaması:
-Büyüme Aşaması: 3-4 yapraklı dönem (BBCH 13-14 (Uwe Meier)).
-Metod: Kök bölgesine enjeksiyon, damla sulama sistemi entegrasyonu.
-Doz: Bitki türüne göre doz kalibrasyonu.
-Tekrar: İlk uygulamadan 14-21 gün sonra booster doz (0.5 mL/bitki).
Çiçeklenme Öncesi Uygulaması:
-Generatif aşamaya geçiş öncesinde (BBCH 50-55).
-Doz: Bitki türüne göre doz kalibrasyonu.
-Amaç: Çiçek ve meyve gelişimi sırasında stres toleransının sağlanması.
Yaprak Püskürtmesi (Foliar Application):
-Sabah erken saatlerde (06:00-09:00) veya akşam saatlerinde (17:00-20:00) yapılır.
-Stoma açıklığının maksimum olduğu dönemler tercih edilir.
-Doz: 200-300 L/ha sıvı hacmi, %0.1-0.2 aktif madde konsantrasyonu.
-Surfaktant eklenerek yaprak yüzey gerilimi azaltılır.
3.4.2Epigenetik değişikliklerin temporal dinamikleri
0-24 Saat:
-Nanopartiküllerin bitki hücrelerine alımı.
-Sitoplazmada epigenetik modülatörlerin salınımı.
-İlk moleküler değişiklikler: histon asetilasyonunda hızlı artış (2-4 saat içinde).
24-72 Saat:
-DNA metilasyon paternlerinde değişiklikler.
-Hedef genlerin kromatin yapısında açılma.
-Transkripsiyon faktörlerinin promotör bölgelerine erişiminde artış.
72 Saat – 7 Gün:
-Gen ekspresyon profillerinde belirgin değişiklikler.
-Protein sentezinde artış (ABA, aquaporinler, LEA proteinleri).
-Metabolik yeniden programlama.
7-30 Gün:
-Fizyolojik adaptasyonların tam olarak yerleşmesi.
-Stres yanıt kapasitesinde maksimum artış.
-Fenotipik değişikliklerin gözlenmesi (kök/gövde oranı, yaprak alanı).
30 Gün – 6 Ay:
-Epigenetik “hafızanın” sürdürülmesi.
-Tekrarlayan stres olaylarına karşı daha hızlı yanıt.
-Bazı metilasyon paternlerinin mitotik kalıtımı.
6-12 Ay:
-Epigenetik işaretlerin kademeli olarak silinmesi.
-Doğal epigenetik dinamiklere geri dönüş.
-Kalıcı genetik değişiklik olmadan normal fenotipin restorasyonu.
3.5Validasyon ve Etkinlik Ölçümü
3.5.1Moleküler düzey validasyonu
Bisülfit Sekanslama:
-Hedef gen promotörlerinde CpG, CHG, CHH metilasyon paternlerinin haritalanması.
-Uygulama öncesi ve sonrası (3, 7, 14, 30 gün) karşılaştırmalı analiz.
-Beklenen sonuç: Hedef genlerin promotörlerinde %20-40 metilasyon azalması.
ChIP-qPCR ve ChIP-seq:
-H3K4me3, H3K9ac, H3K27me3 ve diğer histon modifikasyonlarının lokus-spesifik ölçümü.
-Uygulama sonrası 24-72 saat aralığında maksimum değişiklikler beklenir.
RT-qPCR ve RNA-seq:
-Hedef genlerin mRNA seviyelerinin kantitasyonu.
-Zamana bağlı gen ekspresyon profillerinin oluşturulması.
-Beklenen sonuç: NCED3, PIP1/2, RD22, RD29A, SOS1 gibi genlerde 2-10 kat ekspresyon artışı.
Proteomik Analizler:
-2D-PAGE veya LC-MS/MS ile protein ekspresyon değişikliklerinin tespiti.
-ABA, prolin, şekerler gibi metabolitlerin HPLC veya GC-MS ile ölçümü.
3.5.2Fizyolojik ve fenotipik karakterizasyon
Su İlişkileri:
-Yaprak su potansiyeli (pressure chamber ile).
-Stoma iletkenliği (porometri ile).
-Transpirasyon hızı ve su kullanım etkinliği (WUE).
Fotosentetik Performans:
-Klorofil floresans parametreleri (Fv/Fm, ΦPSII, NPQ).
-Net fotosentez hızı (infrared gas analyzer ile).
İyon Homeostazı (Tuz Stresi):
-Yaprak ve kök dokularında Na⁺, K⁺, Ca²⁺, Cl⁻ konsantrasyonları (ICP-MS veya iyon kromatografisi).
-K⁺/Na⁺ oranı hesaplaması.
Morfolojik ve Büyüme Parametreleri:
-Bitki boyu, yaprak alanı indeksi (LAI).
-Kök/gövde oranı.
-Kuru madde birikimi.
Verim Bileşenleri:
-Tohum/meyve sayısı ve ağırlığı.
-Bin tane ağırlığı.
-Hasat indeksi.
3.5.3Çevresel risk değerlendirmesi
Hedef Dışı Etkiler:
-Genom genelinde DNA metilasyon değişikliklerinin haritalanması (WGBS).
-Transpozon aktivasyonunun izlenmesi.
-Gelişimsel anomalilerin gözlenmesi.
Kalıntı Analizleri:
-Toprakta ve bitki dokularında epigenetik modülatör kalıntılarının HPLC-MS ile tespiti.
-Biyodegradasyonun izlenmesi.
-Yer altı sularına sızma potansiyelinin değerlendirilmesi.
Hedef Dışı Organizmalara Etkiler:
-Toprak mikrobiyom kompozisyonunda değişikliklerin 16S rRNA ve ITS amplikon sekanslama ile analizi.
-Yararlı böcekler (arılar, predatör böcekler) üzerine toksisite testleri.
-Toprak faunası (solucanlar, nematodlar) üzerine etkiler.
- RNAi VE MİKROBİYOM ENTEGRASYONU
4.1 Virüs Benzeri Partiküller (VLP) ile RNAi Teknolojisi
4.1.1VLP tasarımı ve üretimi
Virüs benzeri partiküller (VLP), viral yapısal proteinlerden oluşan ancak genetik materyal içermeyen, kendi kendine organize olan nanostrüktürlerdir. VLP’ler, doğal virüslerin hücre içine giriş yeteneklerini korurken, replikasyon ve enfeksiyon riski taşımaz.
VLP Platformu Seçimi:
PEDAS sisteminde kullanılan VLP’ler, bitki viruslarından türetilen kapsid proteinlerine dayanmaktadır:
1.Cowpea Mosaic Virus (CPMV) VLP:
-İkosaedral geometri, ~30 nm çap.
-Kapsid, VP60 ve VP24 proteinlerinden oluşur.
-Yüksek stabilite ve bitki hücrelerine etkili penetrasyon.
-Genetik mühendisliği kolay; heterolog peptidlerin yüzeyde sunulması mümkün.
2.Tobacco Mosaic Virus (TMV) VLP:
-Çubuk şekilli, 300 nm uzunluk, 18 nm çap.
-Tek kapsid proteini (CP).
-Yüksek yükleme kapasitesi (siRNA başına 2000’den fazla kapsid proteini).
3.Bacteriophage MS2 VLP:
-Prokaryotik kökenli ancak bitki hücrelerine adapte edilmiştir.
-Dimerik kapsid proteini ile 180 kapsid proteini içeren 27 nm partikül.
VLP Üretim Sistemi:
-Heterolog Ekspresyon: E. Coli veya maya (Pichia pastoris) sistemlerinde kapsid proteinlerinin üretimi. Yüksek verim ve ekonomik üretim sağlar (Fuenmayor ve ark., 2017; Cervera ve ark., 2019)..
-Bitki Tabanlı Üretim: Nicotiana benthamiana kullanılarak geçici ekspresyon sistemi (agroinfiltrasyon). Doğru katlama ve post-translasyonel modifikasyonlar sağlar (Gleba ve ark., 2005; Sainsbury ve Lomonossoff, 2008).
siRNA Yükleme:
-Elektrostatik Etkileşim: Pozitif yüklü rezidüler (Arg, Lys) içeren modifiye kapsid proteinleri, negatif yüklü siRNA ile elektrostatik olarak etkileşir (Bruckman ve ark., 2008; Strable ve ark., 2008).
-Paketleme Sinyali (Pac Site) Mühendisliği: TMV’de doğal olarak bulunan “packaging signal” (pac site) modifiye edilerek, siRNA’nın VLP içine spesifik olarak yüklenmesi sağlanır (Osman ve ark., 2006; Kadri ve ark., 2013).
-Kimyasal Konjugasyon: Kapsid proteinlerine tiol (sistein) veya amino reaktif (lizin) gruplar eklenerek, siRNA’ya kovalent bağlanma sağlanır (Stephanopoulos ve ark., 2010; Tong ve ark., 2009).
Karakterizasyon:
-Transmisyon Elektron Mikroskobu (TEM): VLP morfolojisi ve siRNA kapsülasyonu görselleştirilir.
-Dinamik Işık Saçılımı (DLS): Hidrodinamik çap ve boyut homojenliği.
-Elektroforetik Mobilite Shift Assay (EMSA): siRNA yükleme etkinliğinin doğrulanması.
-Enkapsülasyon Verimliliği: Fluoresan etiketli siRNA kullanılarak ölçülür. Hedef: >70%.
4.1.2Hedef patojen belirleme ve siRNA tasarımı
Hedef Patojenler:
PEDAS sisteminde öncelikli hedefler:
1.Fungal Patojenler:
-Fusarium oxysporum (solgunluk hastalığı)
-Botrytis cinerea (gri küf)
-Phytophthora infestans (geç yanıklık)
2.Viral Patojenler:
-Tomato Yellow Leaf Curl Virus (TYLCV)
-Potato Virus Y (PVY)
3.Bakteriyel Patojenler:
-Pseudomonas syringae
-Xanthomonas spp.
siRNA Tasarım Prensipleri:
Etkili RNAi için siRNA tasarımı kritiktir:
-Hedef Gen Seçimi:
-Patojen için esansiyel genler (haustorium formation, toxin synthesis, cell wall degradation enzymes).
-Korunmuş sekanslar (phylogenetic olarak yakın patojenlerde ortak bölgeler).
-Konakçı bitkide homolog olmayan genler (hedef dışı etkileri minimize etmek için).
-siRNA Sekans Özellikleri:
-21-23 nükleotid uzunluğu.
-GC içeriği %30-52 aralığında.
-5’ ucunda “U” tercihi, antisense strand olarak rehber strand seçilimini artırır.
-Internal stability: 3’ uçta düşük termal stabilite (A/U zengin), 5’ uçta yüksek stabilite.
-Off-target homoloji kontrolü: BLAST analizi ile konakçı ve yararlı organizmalardaki homologlar taranır.
Örnek Hedef: Botrytis cinerea BcPG1 (Polygalacturonase):
Botrytis cinerea'nın virulansında kritik bir rol oynar ve hücre duvarı degradasyonunda görev alır.
-siRNA Dizisi (21-mer):
-Sense strand: 5'-GACUUCAAGCUGCUGAACATT-3'
-Antisense strand: 5'-UGUUCAGCAGCUUGAAGUCTT-3'
-Modifikasyonlar:
-2'-O-Metil modifikasyonu: RNaz degradasyonunu yavaşlatır.
-Fosforotiyoat bağları: Nükleazlara karşı direnç artırır.
4.1.3VLP-RNAi uygulama stratejisi
Foliar Application (Yaprak Uygulaması):
VLP-siRNA kompleksleri, yaprak yüzeyine püskürtülür:
-Formülasyon: 10-50 µg siRNA/mL konsantrasyonda, sürfaktan içeren su bazlı süspansiyon.
-Uygulama Zamanı: Hastalık belirtilerinin ilk görüldüğü anda veya enfeksiyon riski yüksek olduğunda (hava koşulları, epidemiyolojik modeller).
-Frekans: 7-10 gün aralıklarla, hastalık baskısına bağlı olarak 2-4 uygulama.
Kök Drench (Toprak Uygulaması):
Toprak kökenli patojenler için:
-Doz: 100-200 µg siRNA/bitki.
-Metod: Damla sulama sistemi ile kök bölgesine iletim.
-Zamanlama: Dikim öncesi veya erken büyüme aşamalarında profilaktik uygulama.
Bitki Hücresine Alım Mekanizması:
VLP'ler, bitki hücresine çeşitli yollarla girer:
-Stoma Girişi: Stoma açıklıkları (5-30 µm), VLP'lerin (20-300 nm) apoplastik boşluğa girişine izin verir.
-Hücre Duvarı Penetrasyonu: Küçük boyut (20-50 nm) ve yüzey modifikasyonları (cell-penetrating peptides), hücre duvarından geçişi kolaylaştırır.
-Endositozis: Plazma membran reseptörleri ile VLP etkileşimi sonucu klathrin veya kaveolaların aracılık ettiği endositozis.
Hücre İçi siRNA Salınımı:
-VLP'ler endozom içinde asidik pH nedeniyle destabilize olur.
-siRNA, endozomdan sitoplazmaya salınır.
-Salınan siRNA, RISC kompleksine yüklenir ve hedef patojen mRNA'sını tanır.
Host-Induced Gene Silencing (HIGS) vs. Spray-Induced Gene Silencing (SIGS):
-HIGS: Konakçı bitkinin siRNA ekspresyonu için transgenikliği gerektirir (GDO).
-SIGS: Eksojen siRNA uygulaması, GDO gerektirmez; PEDAS bu yaklaşımı kullanır.
4.1.4Etkinlik ve spesifiklik
Beklenen Sonuçlar:
-Hastalık İnsidensinde Azalma: %50-70 oranında enfekte bitki sayısında düşüş.
-Hastalık Şiddetinde Azalma: Lezyon boyutunda %40-60 küçülme.
-Patojen Biyomasında Azalma: qPCR ile patojen DNA/RNA kantitasyonunda %60-80 azalma.
Spesifiklik ve Hedef Dışı Etkiler:
-siRNA tasarımı sırasında yapılan bioinformatik analizler, hedef dışı etkileri minimize eder.
-Konakçı bitki genomunda 18 nükleotidden fazla homoloji olmayan diziler seçilir.
-Yararlı mikroorganizmalar (Rhizobia, mikorizal funguslar) üzerine toksisite testleri yapılır.
Direnç Gelişimi:
-RNA tabanlı teknolojiler, dirence karşı daha az yatkındır çünkü hedef sekanslar kolayca değiştirilebilir.
-Multiplexing: Aynı anda birden fazla hedef gene karşı siRNA kokteyli kullanımı, direnç gelişimini zorlaştırır.
4.2Faydalı Mikrobiyom İnokulasyonu
4.2.1Mikrobiyom profilleme ve suş seçimi
Rizosfer Mikrobiyom Analizi:
Hedef mahsul ve lokasyon için mevcut rizosfer mikrobiyomunun karakterizasyonu:
-16S rRNA Gen Sekanslama (Bakteriler): Bakteri topluluklarının taksonomik kompozisyonunu ortaya çıkarır. Illumina MiSeq veya PacBio platformları kullanılır.
-ITS Region Sekanslama (Funguslar): Fungal toplulukların taksonomisini tanımlar.
-Metagenomik Sekanslama: Fonksiyonel gen repertuarını (azot fiksasyonu, fosfat çözünme, antimikrobiyal metabolit sentezi) belirler.
-İzolasyon ve Kültürleme: Dilüsyon plating, selektif medyalar (örneğin NFb medium for Azospirillum, King's B medium for Pseudomonas) kullanarak suşlar izole edilir.
Suş Seçim Kriterleri:
1.Stres Toleransı: İlgili abiyotik stres koşullarında (kuraklık, tuzluluk, soğuk) canlılığını koruyan suşlar.
2.Bitki Büyüme Teşvik Özellikleri:
-IAA (Indole-3-Acetic Acid) üretimi.
-ACC (1-Aminocyclopropane-1-Carboxylic Acid) deaminase aktivitesi (etilen seviyelerini düşürerek stres yanıtını modüle eder).
-Siderafor üretimi (demir alımı).
-Fosfat çözünme aktivitesi.
2.Biyokontrol Kapasitesi:
-Antimikrobiyal metabolit üretimi (surfaktin, iturin, fengycin gibi lipopeptidler).
-Lytic enzyme production (chitinase, glucanase).
3.Kök Kolonizasyon Yeteneği: Bitki köküne etkili bir şekilde bağlanma ve kolonize etme kapasitesi.
Seçilmiş Suşlar:
-Bacillus subtilis GB03: IAA ve surfaktin üretir, kuraklık toleransı artırır.
-Pseudomonas fluorescens CHAO: Antimikrobiyal metabolitler (2,4-diacetylphloroglucinol) üretir, biyokontrol ajanı.
-Azospirillum brasilense Sp245: Azot fiksasyonu, IAA üretimi, kök gelişimini teşvik eder.
-Trichoderma harzianum T22: Mycoparasitism (fungal patojenlere karşı), ISR indüksiyonu.
-Glomus intraradices (Rhizophagus irregularis): AMF, fosfor alımı, kuraklık toleransı.
4.2.2Akıllı mikrokapsülasyon teknolojisi
Faydalı mikroorganizmaların canlılığını korumak ve kontrollü salınım sağlamak için mikrokapsülasyon uygulanır (Burgain ve ark., 2011; Martin ve ark., 2015).
Enkapsülasyon Materyalleri:
1.Aljinat:
-Doğal polimerijnatdır, deniz yosunlarından elde edilir.
-Ca²⁺ iyonları ile çapraz bağlanarak hidrojel oluşturur.
-Biyouyumlu ve biyodegredable.
-Gözenek boyutu, mikroorganizmaların çıkışına izin verirken koruma sağlar.
2.Kitosan:
-Katyonik polimerijnatdır, kitin'in deasetilasyonundan elde edilir.
-Antimikrobiyal özellikleri vardır ve enkapsüle edilen suşların korunmasını destekler.
-pH duyarlı: asidik koşullarda çözünürlüğü artar.
3.Pektin:
-Anionik polimerijnatdır.
-Kalsiyum veya alüminyum iyonları ile jel oluşturur.
Mikrokapsül Formülasyonu:
-Aljinat-Kitosan Çift Kaplama:
-İç çekirdek: %2-3 sodyum aljinat çözeltisinde süspanse mikroorganizmalar.
-Damlama yöntemi ile CaCl₂ çözeltisine damlatılarak sferik jel partiküller oluşturulur (2-4 mm çap).
-Kitosan kaplama: %0.1-0.5 kitosan çözeltisinde (pH 5.5) kaplama, mekanik stabilitenin artırılması.
-Kurutma: Oda sıcaklığında veya düşük sıcaklık kurutma (liyofilizasyon).
Kontrollü Salınım Mekanizması:
-Toprak Nemi Duyarlı Salınım: Kuru koşullarda mikrokapsüller stabil kalır. Toprak nemi arttığında (sulama veya yağış sonrası), hidrojel şişer ve gözenek boyutu genişler, mikroorganizmalar salınır.
-pH Duyarlı Salınım: Rizosfer pH değişiklikleri (kök eksudatlarının etkisiyle asidik pH) kitosan tabakasının çözünmesini tetikler.
-Enzimatik Degradasyon: Topraktaki alginat liyaz ve kitinaz enzimleri, mikrokapsül matriksini yavaş yavaş degrede eder ve sürekli salınım sağlar.
Canlılık Koruması:
-Enkapsülasyon, mikroorganizmaları çevresel streslerden (UV ışınları, kurulukluk, toksik bileşikler) korur.
-Depolama stabilitesi: 4°C'de 6-12 ay canlılık korunur.
-Canlılık testleri: Enkapsülasyon öncesi ve sonrası koloni oluşturan birimler (CFU) sayılır. Hedef: >80% canlılık korunması.
4.2.3Mikrobiyom-bitki-epigenetik etkileşimi
Sinerjistik Etkiler:
Epigenetik programlama ve mikrobiyom inokulasyonunun kombinasyonu sinerjistik etkiler yaratır:
1.Epigenetik Priming + Mikrobiyom:
-Epigenetik olarak programlanmış bitkiler, mikrobiyom kolonizasyonuna daha duyarlı hale gelir.
-Simbiyoz oluşumu için gerekli genlerin (SYMRK, DMI gibi) epigenetik aktivasyonu, mikorizal enfeksiyonu hızlandırır.
2.Mikrobiyal Metabolitler ve Epigenetik Modulasyon:
-Bacillus subtilis tarafından üretilen butirat, HDAC inhibitörü olarak çalışır ve epigenetik programlamayı destekler.
-Mikrobiyal sideraforlar, demir homeostazını düzenleyen genlerde epigenetik değişiklikler indükler.
3.Sistemik Direnç (ISR) ve Epigenetik Hafıza:
-PGPR kaynaklı ISR indüksiyonu, savunma genlerinde kromatin modifikasyonlarına yol açar.
-Bu modifikasyonlar, epigenetik hafıza oluşturarak uzun süreli savunma priming'i sağlar.
Mikrobiyom Stabilizasyonu:
-Epigenetik programlama, bitkilerin kök eksudatlarında değişiklikler yaratabilir.
-Bu değişiklikler, rizosfer mikrobiyom kompozisyonunu şekillendirir ve faydalı mikroorganizmaların zenginleşmesini destekler.
-"Holobiont" perspektifi: Bitki + mikrobiyom bir süper-organizma olarak düşünülür ve PEDAS bu sistemin optimizasyonunu hedefler.
4.2.4İnokulasyon protokolü
Uygulama Zamanı ve Metodu:
1.Tohum Kaplama (Seed Coating):
-Tohum ekiminden önce, mikrokapsül süspansiyonu ile tohum kaplanır.
-Doz: 10⁶-10⁷ CFU/tohum.
-Faydalar: Erken kolonizasyon, çimlenme aşamasında koruma.
2.Toprak İnokulasyonu:
-Dikim sırasında veya erken büyüme aşamalarında, mikrokapsül granülleri toprağa karıştırılır.
-Doz: 1-5 kg/ha (10⁸-10⁹ CFU/g içeren granüller).
3.Damla Sulama ile İnokulasyon:
-Sıvı inokulant formülasyonu (mikrokapsüller süspansiyon halinde) damla sulama sistemi üzerinden verilir.
-Doz: 10⁸-10⁹ CFU/bitki, erken büyüme döneminde 2-3 uygulama.
Kalite Kontrol:
-Her parti inokulantın CFU, saflık (contamination testi) ve fizyolojik aktivite (IAA üretimi, fosfat çözünme) testleri yapılır.
-Raf ömrü testleri: 3, 6, 9, 12 ay depolama sonrası canlılık kontrolü.
4.3RNAi ve Mikrobiyom Entegrasyonunun Doğrulanması
4.3.1Sera ve çiftlik denemeler
Kontrollü Sera Denemeleri:
-Deneysel Tasarım: Randomize blok dizaynı, 4 tekrarlı, her tekrarda 10 bitki.
-Muamele Grupları:
1.Kontrol (işlem görmemiş)
2.Sadece VLP-RNAi
3.Sadece mikrobiyom inokulasyonu
4.VLP-RNAi + mikrobiyom (PEDAS tam sistemi)
5.Konvansiyonel fungisit/pestisit (karşılaştırma için)
-Patojen İnokulasyonu: Yapay enfeksiyon, standart patojen suşları ile (Botrytis cinerea spor süspansiyonu 10⁵ spor/mL).
-Değerlendirme Parametreleri:
-Hastalık şiddeti skoru (0-5 skalası).
-Lezyon alanı (Image analysis yazılımı ile).
Patojen biyomas (qPCR ile patojen DNA kantitasyonu).
-Bitki büyüme parametreleri (boy, biyomas).
Açık Arazi Denemeleri:
-Lokasyonlar: Farklı iklim ve toprak koşullarını temsil eden çoklu lokasyonlar (en az 3).
-Parsel Boyutu: 50-100 m² parsel, 4 tekrarlı.
-Doğal Patojen Baskısı: Yapay inokulasyon yerine, doğal enfeksiyon koşullarında etkinlik değerlendirmesi.
-Verim ve Kalite: Hasat sonrası verim (kg/ha), pazar değeri, besin içeriği analizleri.
4.3.2Moleküler ve mikrobiyolojik analizler
Patojen Gen İfadesinin Takibi:
-RT-qPCR ile hedef patojen genlerinin (örneğin Botrytis BcPG1) ekspresyon seviyelerinin ölçülmesi.
-SIGS uygulama sonrası 24, 48, 72 saat ve 7 gün aralıklarında numune alınır.
-Beklenen sonuç: Hedef gen ekspresyonunda %60-80 azalma.
Mikrobiyom Profil Değişiklikleri:
-16S rRNA gen sekanslama ile rizosfer bakteriyel topluluk kompozisyonunun izlenmesi.
-İnokulasyon öncesi ve sonrası (2, 4, 8 hafta) karşılaştırma.
-Beklenen sonuç: İnokule edilen suşların rizosfer topluluğunda baskın hale gelmesi (%5-20 relatif bolluk).
Fonksiyonel Mikrobiyom Analizi:
-Metagenomik ve meta-transkriptomik sekanslama ile fonksiyonel gen ekspresyonunun incelenmesi.
-Azot fiksasyonu (nifH geni), fosfat çözünme (pqqE geni) ve antimikrobiyal sentez (NRPS/PKS genleri) aktivitesinin doğrulanması.
4.3.3Uzun vadeli izleme
Çok Yıllı Etkiler:
-Mikrobiyom inokulasyonunun ertesi sezon etkilerinin değerlendirilmesi.
-Toprak mikrobiyom kalitesinde iyileşmelerin takibi.
Direnç Gelişimi Sürveyansı:
-Hedef patojenlerde RNAi direnci gelişiminin moleküler izlenmesi.
-Sezon içi ve sezonlar arası örnekleme ile patojen populasyonlarında hedef gen sekanslarının analizi.
- IoT VE YAPAY ZEKA ENTEGRASYONU
5.1 Akıllı Sensör Ağı Altyapısı
5.1.1Donanım bileşenleri
Sensör Node Tasarımı:
Her sensör node'u, aşağıdaki bileşenlerden oluşur:
-Mikrocontroller: ARM Cortex-M serisinde düşük güç tüketimli MCU (örneğin STM32L4 serisi).
-Sensör Modülleri: I2C veya SPI protokolleri ile mikrocontrollera bağlı sensörler (toprak nemi, sıcaklık, EC, pH).
-Güç Yönetimi: Güneş paneli (5W) + Li-ion batarya (10,000 mAh) kombinasyonu. Enerji hasadı (energy harvesting) ile sürekli çalışma.
-İletişim Modülü:
-LoRaWAN: Uzun menzil (5-15 km açık alanda), düşük güç, düşük veri hızı. Tarla ölçeğinde dağıtık sensör ağları için ideal.
-NB-IoT: Hücresel altyapı kullanır, daha geniş kapsama, biraz daha yüksek güç tüketimi.
-Veri Depolama: Yerel SD kart (bağlantı kesildiğinde veri kaybını önler).
Gateway ve Baz İstasyonu:
-Sensör node'larından gelen verileri toplar ve bulut sunucusuna iletir.
-3G/4G/5G veya ethernet bağlantısı.
-Edge computing kapasitesi: bazı ön-işlemeler (filtreleme, aggregation) gateway seviyesinde yapılır.
5.1.2Veri toplama ve ön işleme
Veri Akışı:
1.Sensörler her 15-30 dakikada bir okuma yapar (enerji tasarrufu için programlanabilir aralık).
2.Veriler yerel olarak timestamp ve GPS koordinatları ile etiketlenir.
3.LoRaWAN ağı üzerinden gateway'e iletilir.
4.Gateway, verileri paketler ve bulut sunucusuna gönderir (MQTT veya HTTPS protokolü).
Veri Kalite Kontrolü:
-Outlier Detection: İstatistiksel yöntemler (z-score, IQR) ile anormal değerler tespit edilir ve flag'lenir.
-Missing Data Imputation: Zaman serisi interpolasyon teknikleri (linear, spline) kullanılarak eksik veriler tamamlanır.
-Sensor Calibration: Periyodik olarak (ayda bir), referans ölçümler ile sensör kalibrasyonu doğrulanır.
5.1.3Bulut veri platformu
Mimari:
-Database: Time-series database (InfluxDB, TimescaleDB) kullanılır; sensör verilerinin etkin depolanması ve sorgulanması.
-Data Warehouse: Uzun vadeli analitik için tarihsel veriler (birkaç yıllık) depolanır.
-API Gateway: RESTful API'ler ile veri erişimi ve entegrasyon.
Veri Güvenliği:
-TLS/SSL şifrelemesi ile veri iletimi.
-Rol tabanlı erişim kontrolü (RBAC).
-GDPR ve veri gizliliği regülasyonlarına uyum.
5.2Makine Öğrenmesi ve Tahmin Modelleri
5.2.1Stres tahmin modelleri
Kuraklık Stresi Tahmini:
-Girişler:
-Toprak nem profili (birden fazla derinlikte).
-Meteorolojik tahminler (sıcaklık, yağış, buharlaşma, rüzgar hızı).
-Bitki fenolojik aşama.
-Tarihsel toprak nem trendleri.
-Model Tipi:
-LSTM (Long Short-Term Memory) Ağları: Zaman serisi tahminleri için güçlü. Toprak nem dinamiklerinin temporal bağımlılıklarını yakalayabilir.
-Gradient Boosting (XGBoost, LightGBM): Tabular veri için yüksek performans. Feature engineering ile meteorolojik ve toprak verilerinin kombinasyonu.
-Çıkış:
-Gelecekteki 3-7 günlük periyotta kuraklık stres skoru (0-1, 0: stres yok, 1: şiddetli stres).
-Güven aralıkları (credible intervals) ile belirsizlik tahmin edilir.
-Model Eğitimi:
-Tarihsel veriler (3-5 yıllık) ile supervised learning.
-Eğitim seti: %70, validasyon: %15, test: %15.
-Performans metrikleri: RMSE (Root Mean Square Error), MAE (Mean Absolute Error), R² (Coefficient of Determination).
Hastalık Risk Tahmini:
-Girişler:
-Yaprak ıslaklık süresi.
-Sıcaklık ve nem (hastalık gelişimi için uygun koşullar).
-Bitki büyüme aşaması (hassasiyet değişir).
-Geçmiş hastalık vaka kayıtları.
-Model Tipi:
-Random Forest Classifier: Binary classification (hastalık riski yüksek/düşük).
-Epidemiyolojik Modeller (SIR benzeri): Hastalık yayılım dinamiklerinin simülasyonu.
-Çıkış:
-Yüksek risk uyarısı: VLP-RNAi uygulaması önerisi.
-Orta risk: izleme artırılması.
-Düşük risk: rutin işlemler.
5.2.2Doz optimizasyon algoritması
Amaç:
Her bir bitkiye veya parsele özgü, optimal epigenetik modülatör dozajının belirlenmesi.
Parametre Uzayı:
-5-azaC konsantrasyonu: 0-2 µM
-TSA konsantrasyonu: 0-0.5 µM
-Uygulama sıklığı: 1-4 hafta aralıkları
-Uygulama hacmi: 0.5-2 mL/bitki
Çoklu Objektif Optimizasyonu:
-Objektif 1: Verim maksimizasyonu (kg/ha).
-Objektif 2: Girdi maliyeti minimizasyonu ($/ha).
-Objektif 3: Çevre etkisi minimizasyonu (kimyasal kalıntı skoru).
Optimizasyon Metodu:
-Bayesian Optimization: Sample-efficient optimizasyon yöntemi. Gaussian process (GP) modelleri ile parametre uzayının keşfi.
-Pareto Frontu: Çoklu objektif optimizasyonunda, trade-off'ları gösteren optimal çözüm seti belirlenir.
-Reinforcement Learning (İleri Düzey): Agent, tarla koşullarını gözlemler (state) ve eylem (doz) seçer. Reward, verim artışı ve maliyet azalması kombinasyonudur. Zaman içinde optimal politika öğrenir.
5.2.3Model güncellemesi ve adaptasyon
Online Learning:
-Yeni verilerin geldikçe modelin incremental olarak güncellenmesi.
-Her sezon sonunda, model parametreleri yeniden eğitilir (seasonal retraining).
Transfer Learning:
-Bir lokasyonda/mahsulda eğitilmiş model, diğer lokasyonlara/mahsullere adapte edilir.
-Domain adaptation teknikleri ile farklı çevresel koşullardaki performans artırılır.
Model Explainability:
-SHAP(SHapley Additive exPlanations) değerleri ile modelin tahminlerini açıklama.
-Çiftçilere hangi faktörlerin (örneğin toprak nemi, sıcaklık) tahminleri en çok etkilediğini gösterme.
5.3Otonom Karar ve Uygulama Sistemi
5.3.1Karar ağacı ve kural tabanlı sistem
Makine öğrenmesi tahminleri, kural tabanlı bir karar sistemi ile birleştirilir:
Örnek Karar Akışı:
IF kuraklık_stres_tahmini > 0.7 (yüksek risk)
AND toprak_nemi < eşik_değeri
AND uygulama_sonrası_geçen_süre > 14 gün
THEN:
-Epigenetik modülatör uygulama başlat
-Doz: optimize_edilmiş_doz(bitki_yaşı, toprak_tipi)
-Log: uygulama kaydı
ELSE IF hastalık_riski == "yüksek"
AND VLP_RNAi_stok > minimum_seviye
THEN:
-VLP-RNAi uygulaması başlat
-Hedef patojen: [tespit_edilen_patojen]
ELSE:
-Rutin izleme devam et
Güvenlik Kontrolleri:
-Maksimum uygulama sıklığı kontrolü (over-application önleme).
-Minimum stok seviyesi kontrolü (kimyasal eksikliğinde uyarı).
-Çevresel koşul kontrolü (rüzgar hızı, yağış tahmini; uygulama geciktirme).
5.3.2Otomatik dozaj kontrol ünitesi
Donanım:
-Peristaltik Pompalar: Hassas sıvı dozajı (±2% hata payı). Her bir kimyasal için ayrı pompa hattı.
-Karıştırma Tankı: Formülasyonun hazırlanması, pH ve EC ayarı.
-Damla Sulama Entegrasyonu: Mevcut sulama sistemine modüler bağlantı. Solenoid vanalar ile parsellere dağıtım kontrolü.
-Akış Sensörleri: Uygulanan dozun gerçek zamanlı doğrulaması.
Yazılım:
-PLC (Programmable Logic Controller) veya Raspberry Pi/Arduino bazlı kontrol sistemi.
-Bulut sunucusu ile RESTful API ile iletişim: uygulama komutlarını alır, gerçek zamanlı geri bildirim gönderir.
-Lokal fail-safe mekanizmaları: İletişim kesilirse, önceden tanımlı güvenli duruma geçiş.
Uygulama Prosedürü:
1.Sistem, bulut sunucusundan "uygulama komutu" alır (parsel ID, kimyasal tipi, doz, zaman).
2.Karıştırma tankında formülasyon hazırlanır (kimyasalların pompalanması, su ile dilüsyon).
3.pH ve EC sensörleri ile formülasyon kalitesi doğrulanır.
4.Onay sonrası, solenoid vana açılır ve hedef parsele damla sulama ile verilir.
5.Akış sensörleri ile uygulanan toplam hacim ölçülür ve kaydedilir.
6.Uygulama tamamlandıktan sonra sistem temizlenir (flushing cycle).
5.3.3Kullanıcı arayüzü ve çiftçi entegrasyonu
Web ve Mobil Uygulama:
-Dashboard: Gerçek zamanlı tarla durumu (toprak nemi, sıcaklık, hastalık riski) görselleştirmesi. Harita bazlı gösterim (GIS entegrasyonu).
-Uyarılar ve Bildirimler: Push notifikasyonlar (stres tahmini, uygulama önerileri, sistem bakım uyarıları).
-Manuel Müdahale Seçeneği: Çiftçi, önerilen uygulamaları onaylayabilir veya reddedebilir. Tam otomatik modda, sistem kendi başına uygulama yapar.
-Raporlama: Haftalık/aylık raporlar (uygulama geçmişi, stres olayları, verim tahminleri, maliyet analizi).
Eğitim ve Destek:
-Video eğitim materyalleri: Sistemin kurulumu, bakımı, sorun giderme.
-Chatbot destekli teknik destek: Yaygın soruların otomatik cevaplanması.
-Tarım danışmanlık entegrasyonu: Karmaşık durumlarda uzman ziraat mühendislerine erişim.
5.4Veri Analitikleri ve İş Zekası
5.4.1Performans metrikleri ve KPI'lar
Tarımsal KPI'lar:
-Su Kullanım Etkinliği (WUE): kg ürün / m³ su.
-Kimyasal Girdi Azaltma: PEDAS ile pestisit/fungisit kullanımında % azalma.
-Verim Artışı: Kontrol parseller ile karşılaştırma, % verim artışı.
-Hastalık İnsidensı: Sezondaki hastalık vaka sayısı ve şiddeti.
Ekonomik KPI'lar:
-ROI (Return on Investment): (Net Kazanç - Yatırım Maliyeti) / Yatırım Maliyeti × 100.
-Break-even Analizi: PEDAS sisteminin maliyetinin geri dönüş süresi.
-Birim Üretim Maliyeti: $/kg ürün.
Sürdürülebilirlik KPI'lar:
-Karbon Ayak İzi: kg CO₂ eşdeğeri / ha.
-Azot ve Fosfor Kullanım Etkinliği: Besin elementi kayıplarının azaltılması.
-Toprak Sağlığı İndeksi: Organik madde içeriği, mikrobiyom çeşitliliği, biyolojik aktivite göstergeleri.
5.4.2Uzun vadeli trend analizi
Çok Yıllı Veri Analizi:
-Sezonlar arası karşılaştırma: PEDAS uygulamasının uzun vadeli etkilerinin değerlendirilmesi.
-İklim değişikliği adaptasyonu: Değişen iklim koşullarında sistemin performansının izlenmesi.
Benchmark Analizi:
-Farklı çiftlikler/bölgeler arasında performans karşılaştırması.
-En iyi uygulamaların (best practices) belirlenmesi ve yaygınlaştırılması.
5.4.3Araştırma ve geliştirme için veri madenciliği
Büyük Veri Analitiği:
-Binlerce çiftlikten toplanan verilerin entegre analizi.
-Yeni stres toleransı veya verim ile ilişkili epigenetik biomarkerlerin keşfi.
-Yeni mikrobiyom suşlarının performans analizleri.
Genomik Veri Entegrasyonu (Gelecek Perspektif):
-Bitki genotip verileri ile fenotipik performans ve epigenetik profillerin entegrasyonu.
-Genome-wide association studies (GWAS) ile stres toleransı ile ilişkili genomik bölgelerin tanımlanması.
- HUKUKİ STATÜ VE REGÜLASYON
6.1 GDO-Dışı Statünün Temelleri
6.1.1 Genetik modifikasyon tanımı
Yasal çerçevelerde GDO (Genetik Modifiye Organizm), DNA diziliminde kalıcı ve kalıtsal değişiklik yapılan organizmalar olarak tanımlanır. Avrupa Birliği Direktifi 2001/18/EC'ye göre GDO: "Genetik materyali, doğal yollarla (üreme ve/veya doğal rekombinasyon) gerçekleşmeyen şekilde değiştirilmiş organizmalar."
PEDAS Sistemi ve GDO Ayrımı:
PEDAS sistemi, bitkilerin DNA diziliminde kalıcı bir değişiklik yaratmaz. Epigenetik modifikasyonlar:
-DNA baz dizilimini değiştirmez; sadece gen ekspresyonunu modüle eder.
-Geçicidir ve 6-12 ay içerisinde doğal turnover süreçleri ile silinir.
-Transgenik gen transferi içermez; eksojen DNA eklenmez.
Bu özellikler, PEDAS teknolojisinin GDO kapsamı dışında kalmasını sağlar.
6.1.2 Biyostimülant regülasyonu (EU 2019/1009)
Avrupa Birliği, 2019 yılında biyostimülantlar için yeni bir regülasyon çerçevesi oluşturmuştur: Regulation (EU) 2019/1009 laying down rules on the making available on the market of EU fertilizing products.
Biyostimülant Tanımı (Madde 2):
"Bitkisel biyostimülant: Bitkilerin besin elementi durumundan bağımsız olarak, aşağıdaki özellikleri uyararak bitki veya rizosferlerine uygulanan bir madde veya mikroorganizma:
-Bitki besin elementi kullanım etkinliğini artırma,
-Abiyotik strese toleransı artırma,
-Kalite özelliklerini iyileştirme,
-Toprak besin elementlerinin biyoyararlanımını artırma."
PEDAS Uyumluluğu:
PEDAS sistemi, bu tanıma tam olarak uymaktadır:
-Epigenetik modülatörler, bitkilerin besin kullanım etkinliğini ve stres toleransını artırır.
-Mikroorganizma inokulasyonu, tanımdaki "mikroorganizma" kategorisine girer.
-RNAi uygulaması, bitki kalitesini (patojen hasarını azaltarak) iyileştirir.
Kayıt ve Onay Süreci:
EU 2019/1009 regülasyonu altında, biyostimülantlar Product Function Category (PFC) 6 olarak sınıflandırılır. Onay için:
1.Etkinlik dossyesi: Bilimsel çalışmalar ve tarla testleri sonuçları.
2.Güvenlik dossyesi: Toksikolojik testler, çevresel risk değerlendirmesi, etiketleme bilgileri.
3.Uyumluluk belgesi: CE marking için gerekli dokümantasyon.
6.2 Ulusal ve Uluslararası Regülasyon Manzarası
6.2.1 Avrupa Birliği
EFSA (European Food Safety Authority) Değerlendirmesi:
Yeni biyostimülantlar, EFSA tarafından değerlendirilir:
-İnsan ve hayvan sağlığına risk analizi.
-Çevre etkilerinin değerlendirilmesi (toprak, su, biyoçeşitlilik).
-Kalıntı analizleri ve Maximum Residue Limits (MRL) belirlenmesi (gerekirse).
REACH (Registration, Evaluation, Authorization and Restriction of Chemicals) Uyumluluğu:
Epigenetik modülatörler kimyasal maddeler olarak REACH kapsamına girebilir:
-Yıllık 1 ton üzeri üretim/ithalat için kayıt gereklidir.
-Güvenlik veri sayfaları (SDS) hazırlanmalıdır.
-Risk değerlendirmesi: maruziyet senaryoları, güvenli kullanım koşulları.
6.2.2 Amerika Birleşik Devletleri
EPA (Environmental Protection Agency) Düzenlemeleri:
RNAi bazlı biyopestisitler, EPA tarafından düzenlenir:
-FIFRA (Federal Insecticide, Fungicide, and Rodenticide Act) altında pestisit olarak sınıflandırılabilir.
-RNAi ürünleri genellikle "biochemical pesticides" kategorisindedir ve risk değerlendirmesi nispeten hafiftir.
-PEDAS'ın RNAi modülü, EPA ile ön-danışma (pre-submission consultation) ile kayıt stratejisi belirlenir.
USDA (United States Department of Agriculture) ve APHIS:
Bitki sağlığı ürünleri ve mikrobiyom inokulantlar için:
-Biyolojik kontrol ajanları: APHIS permit veya notifikasyon gerekebilir.
-Endojen (ABD'de doğal olarak bulunan) mikroorganizmalar genellikle permit gerektirmez.
FDA (Food and Drug Administration):
Gıda güvenliği açısından, kalıntı analizleri ve GRAS (Generally Recognized as Safe) statüsü değerlendirmesi yapılır.
6.2.3 Gelişmekte olan ülkeler
Brezilya:
-Tarım Bakanlığı (MAPA) ve ANVISA (sağlık otoritesi) düzenlemeleri.
-Biyolojik girdiler için özel bir kayıt sistemi (Registro de Produtos Biológicos).
-PEDAS, "biológico" kategorisinde değerlendirilebilir.
Hindistan:
-Central Insecticides Board and Registration Committee (CIBRC) düzenlemeleri.
-Biyopestisitler ve biyostimülantlar için ayrı kayıt prosedürleri.
Türkiye:
-Tarım ve Orman Bakanlığı düzenlemeleri.
-Bitki Koruma Ürünleri Yönetmeliği ve Toprak Islahı, Bitki Besleme ve Biyostimülantlar Yönetmeliği.
-PEDAS, biyostimülant olarak kayıt edilebilir.
6.3 Biyogüvenlik ve Çevresel Risk Değerlendirmesi
6.3.1 Çevresel kaderin değerlendirilmesi
Epigenetik Modülatörlerin Geleceğini Belirleme:
-Toprak Absorpsiyonu: Toprak organik maddesi ve kil mineralleri ile etkileşim. Adsorpsiyon katsayıları (Kd) belirlenir.
-Mikrobiyolojik Degradasyon: Toprak mikroorganizmaları tarafından parçalanma hızı. OECD 301 testleri (Biodegradability).
-Fotoliz: Güneş ışığı altında parçalanma. OECD 316 test.
-Yer Altı Sularına Sızma Potansiyeli: Leaching testleri, GUS indeksi (Groundwater Ubiquity Score).
RNAi Moleküllerinin Geleceği:
-dsRNA/siRNA molekülleri, çevresel RNazlar tarafından hızla degrage edilir (yarı ömür: birkaç saat - birkaç gün).
-Toprak partiküllerine adsorpsiyon, degradasyon hızını yavaşlatabilir ancak biyoyararlanımı azaltır.
-Hedef dışı organizmalara maruziyet minimal: spesifik uygulama ve hızlı degradasyon.
VLP Kapsüllerinin Geleceği:
-Protein bazlı VLP'ler, proteolitik enzimler tarafından parçalanır.
-Çevre koşullarında (UV, ısı, nem) stabilitesi sınırlıdır; kontrollü salınım sonrası hızla parçalanır.
6.3.2 Hedef dışı organizmalar üzerine etkiler
Toprak Mikroorganizmaları:
-16S rRNA gen sekanslama ile mikrobiyal topluluk kompozisyonundaki değişiklikler izlenir.
-Fonksiyonel çeşitlilik (enzim aktiviteleri: dehidrogenase, fosfatase, urease) ölçülür.
-Beklenen etki: Minimal değişiklik. İnokule edilen faydalı mikroorganizmaların zenginleşmesi istenir, ancak toplam mikrobiyal çeşitlilik korunmalıdır.
Yararlı Böcekler:
-Arılar (Apis mellifera, Bombus spp.), predatör böcekler (Coccinellidae, Chrysopidae) üzerine toksisite testleri.
-Oral, topikal ve larvaya maruziyet testleri.
-Beklenen sonuç: RNAi spesifik tasarımı sayesinde minimal hedef dışı etki.
Sucul Organizmalar:
-Daphnia magna, balık türleri (zebrafish), algler üzerine toksisite testleri (OECD 201, 202, 203).
-Toprak uygulaması sonrası yüzeysel suya taşınma potansiyeli düşüktür.
Toprak Faunası:
-Solucanlar (Eisenia fetida): OECD 207 (akut toksisite) ve 222 (üreme testi).
-Collembola (Folsomia candida): OECD 232.
6.3.3 Uzun vadeli ekolojik izleme
Monitoring Programı:
-Pilot uygulamaların yapıldığı alanlarda 3-5 yıl süreyle ekolojik izleme.
-Toprak kalitesi parametreleri (organik madde, pH, mikrobiyom çeşitliliği).
-Faydalı ve zararlı böcek populasyonlarının takibi.
-Su kaynaklarında kimyasal kalıntı analizleri.
Adaptif Yönetim:
-İzleme sonuçlarına göre uygulama protokollerinin güncellenmesi.
-Risk-fayda analizinin devamlı olarak yeniden değerlendirilmesi.
6.4 Entelektüel Mülkiyet ve Patentleme
6.4.1 Patent stratejisi
PEDAS sisteminin farklı bileşenleri için kapsamlı patent portföyü:
Patent 1: Epigenetik Programlama Formülasyonu
-Nano-lipit kompleks kompozisyonu.
-Spesifik epigenetik modülatör kombinasyonları ve konsantrasyonları.
-Uygulama metodolojisi ve zamanlama protokolleri.
Patent 2: VLP-RNAi Delivery Sistemi
-VLP tasarımı ve siRNA yükleme yöntemleri.
-Patojen spesifik siRNA dizileri.
-Stabilizasyon formülasyonları.
Patent 3: Mikrokapsülasyon Teknolojisi
-Akıllı mikrokapsül kompozisyonu (aljinat-kitosan).
-Kontrollü salınım mekanizmaları (nem, pH duyarlı).
-Mikroorganizma canlılığını koruyan formülasyon.
Patent 4: IoT ve Yapay Zeka Entegrasyonu
-Sensör ağı mimarisi ve veri akış protokolleri.
-Makine öğrenmesi algoritmaları (stres tahmini, doz optimizasyonu).
-Otomatik dozaj kontrol sistemi.
Patent 5: Entegre Sistem ve Yöntem
-PEDAS sisteminin tamamının entegrasyonu.
-Çoklu stres hedefleyen holistik yaklaşım.
6.4.2 Ticari sır ve know-how
Bazı bilgiler patent yerine ticari sır olarak korunur:
-Spesifik mikrobiyom suşlarının seçim kriterleri ve performans verileri.
-Makine öğrenmesi modellerinin eğitim veri setleri ve hiperparametreleri.
-Çiftlik spesifik optimizasyon protokolleri.
6.5 Etiketleme ve Pazarlama İddiaları
6.5.1 Ürün etiket içeriği
AB regülasyonlarına uygun etiketleme:
-Ürün Adı: PEDAS Epigenetik Bitki Stres Tolerans Sistemi
-Ürün Fonksiyon Kategorisi: PFC 6 - Bitkisel Biyostimülant
-Aktif Bileşenler:
-Epigenetik modülatör kompleksi (5-azaC, TSA).
-Faydalı mikroorganizmalar (suş isimleri ve CFU değerleri).
-RNAi modülü (siRNA hedef bilgileri).
-Kullanım Talimatları: Doz, uygulama zamanı, metod.
-Güvenlik Bilgileri: Güvenli kullanım koşulları, ilk yardım, saklama.
-Çevresel Uyarılar: Hedef dışı etkilerin minimizasyonu için öneriler.
-İrtibat Bilgileri: Üretici firma, teknik destek hattı.
6.5.2 Pazarlama iddiaları
Doğrulanmış İddialar:
-"Kuraklık toleransında %20-40 verim artışı" (tarla denemelerine dayalı).
-"Pestisit kullanımında %50-70 azalma" (RNAi modülü etkinlik verileri).
-"Su kullanım etkinliğinde %40 artış" (WUE ölçümleri).
-"GDO içermez, tamamen doğal süreçleri kullanır" (biyogüvenlik değerlendirmesi).
Reklam ve İletişim:
-Bilimsel temelli iletişim: Peer-reviewed yayınlar, konferans sunumları.
-Çiftçi testimonial'ları ve vaka çalışmaları.
-Sürdürülebilirlik sertifikaları (organic uyumlu, carbon-neutral gibi).
6.6 Coexistence (Bir Arada Yaşama) ve Geçiş Protokolleri
6.6.1 GDO ve konvansiyonel üretim ile bir arada yaşama
PEDAS teknolojisi GDO içermediği için, konvansiyonel ve organik tarım ile bir arada yaşama sorunları minimumdur:
-Buffer Zones (Tampon Bölgeler): Epigenetik modülatörlerin komşu parsellere taşınmasını önlemek için sınırlı tampon bölgeler yeterlidir (örneğin 5-10 m).
-Spray Drift Önlemi: Damla sulama entegrasyonu ve hedefli uygulama, havaya saçılmayı minimize eder.
6.6.2 Organik tarıma geçiş
PEDAS sistemi, organik sertifikasyona geçiş sürecinde de kullanılabilir:
-AB Organic Regulation (EU 2018/848) ve USDA Organic standartlarına uyumluluk.
-Kullanılan tüm bileşenlerin (epigenetik modülatörler, mikroorganizmalar) organik izin listelerinde olması veya muafiyet alınması gerekir.
-Şeffaflık: Tüm girişlerin kaynağının ve işleme yöntemlerinin belgelenmesi.
7.MATERYAL ve YÖNTEM
7.1. İstatistiksel Analiz
Bu çalışmada elde edilen simülasyon verilerinin analizi, çok aşamalı istatistiksel ve çok değişkenli veri analizi yaklaşımı kullanılarak gerçekleştirilmiştir. Tüm analizler Python programlama dili kullanılarak yürütülmüş; veri işleme için NumPy ve Pandas, istatistiksel testler için SciPy ve Statsmodels, makine öğrenmesi analizleri için ise Scikit-learn kütüphanelerinden yararlanılmıştır.
7.1.1. Veri Ön İşleme
Simülasyon çıktıları senaryo bazlı (epigenetik, kontrol, mikrobiyom, RNAi) kategorize edilmiştir. Sürekli değişkenler için:
Ortalama (x̄)
Standart sapma (SD)
Minimum ve maksimum değerler
hesaplanarak betimleyici istatistikler elde edilmiştir.
Analiz öncesinde veri setinde eksik değer kontrolü yapılmış ve simülasyon çıktıları deterministik olduğu için eksik veri bulunmamıştır.
7.1.2. Normallik ve Varyans Homojenliği
Tek yönlü varyans analizinden önce aşağıdaki varsayımlar değerlendirilmiştir:
-Artıkların yaklaşık normal dağılım göstermesi
-Gruplar arası varyans homojenliği
Normallik görsel dağılım incelemeleri ve artık analizleri ile değerlendirilmiş, varyans homojenliği Levene testi ile kontrol edilmiştir. Varsayımlar sağlandığından parametrik testler uygulanmıştır.
7.1.3. Tek Yönlü Varyans Analizi (ANOVA)
Senaryolar arasında istatistiksel olarak anlamlı fark olup olmadığını belirlemek amacıyla tek yönlü ANOVA uygulanmıştır.
Test edilen temel değişkenler:
protein_gen1
bakteri_log
ABA düzeyi
epigenetik parametreler
ANOVA model yapısı:
Yᵢⱼ = μ + τᵢ + εᵢⱼ
Burada:
μ genel ortalamayı,
τᵢ grup etkisini,
εᵢⱼ hata terimini temsil etmektedir.
Anlamlılık düzeyi α = 0.05 olarak belirlenmiştir.
ANOVA sonucunda anlamlı fark saptanan değişkenler için çoklu karşılaştırma amacıyla Tukey HSD (Honestly Significant Difference) testi uygulanmıştır.
7.1.4. Korelasyon Analizi
Değişkenler arası doğrusal ilişkileri incelemek amacıyla Pearson korelasyon katsayısı hesaplanmıştır.
Özellikle aşağıdaki ilişkiler değerlendirilmiştir:
Tuz stresi – SOS1 ekspresyonu
Kuraklık stresi – NCED3 ekspresyonu
Histon asetilasyonu – stres genleri
DNA metilasyonu – stres genleri
Korelasyon katsayıları ısı haritası (heatmap) ile görselleştirilmiştir.
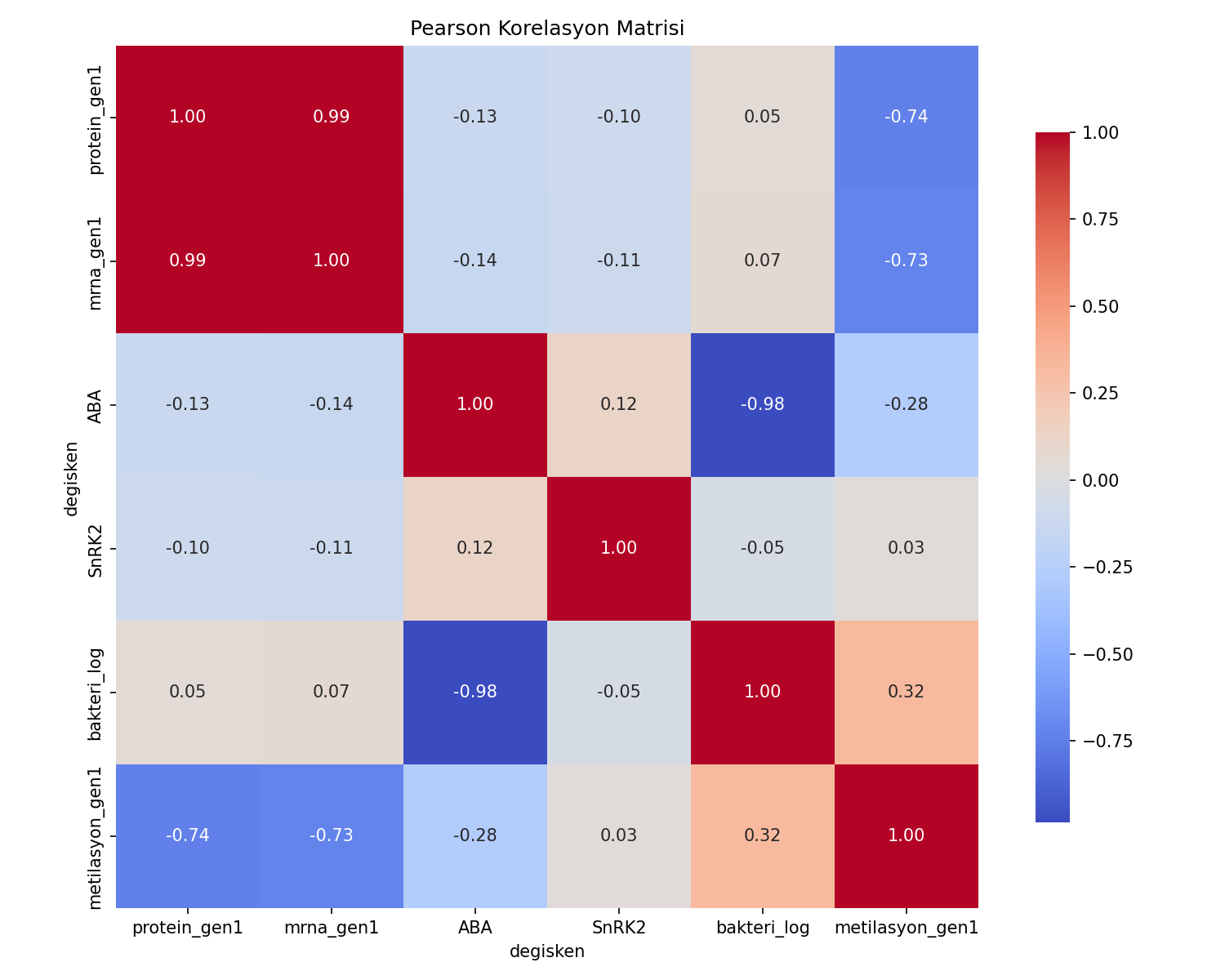
7.1.5. Temel Bileşenler Analizi (PCA)
Veri setinin çok değişkenli yapısını indirgemek ve senaryo bazlı ayrışmayı incelemek amacıyla PCA uygulanmıştır.
Analiz öncesinde değişkenler z-skor standardizasyonu ile ölçeklendirilmiştir. İlk iki temel bileşen üzerinden varyans açıklama oranları hesaplanmış ve senaryoların çok boyutlu uzaydaki konumları görselleştirilmiştir.
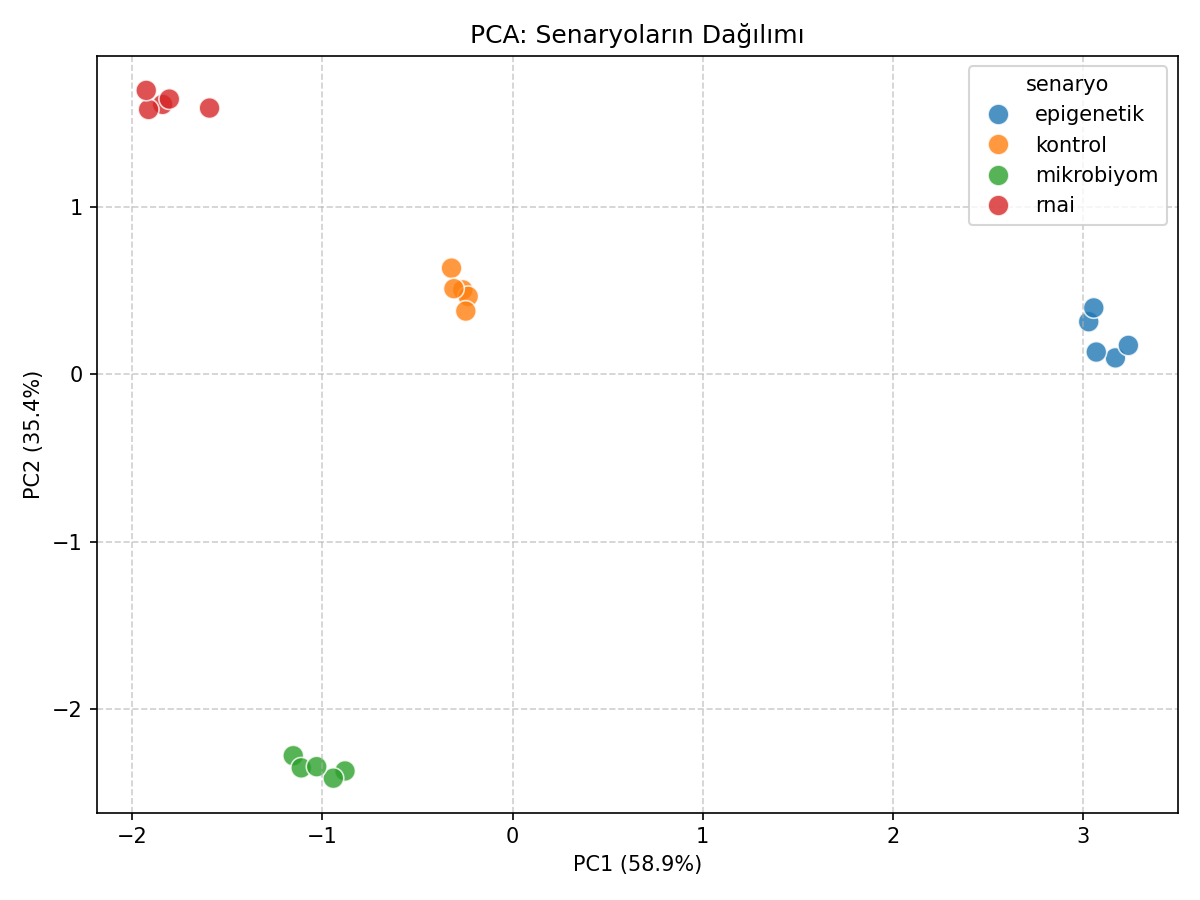
.1.6. Kümeleme Analizi
Verilerin doğal gruplaşma yapısını incelemek amacıyla K-Means kümeleme algoritması uygulanmıştır.
Küme sayısı (k), ön analizler ve senaryo sayısı dikkate alınarak belirlenmiştir.
Küme merkezleri iteratif olarak optimize edilmiştir.
Küme dağılımı grafiksel olarak değerlendirilmiştir.
Bu analiz, model çıktılarının senaryo bazlı yapısal farklılık içerip içermediğini test etmek amacıyla yapılmıştır.
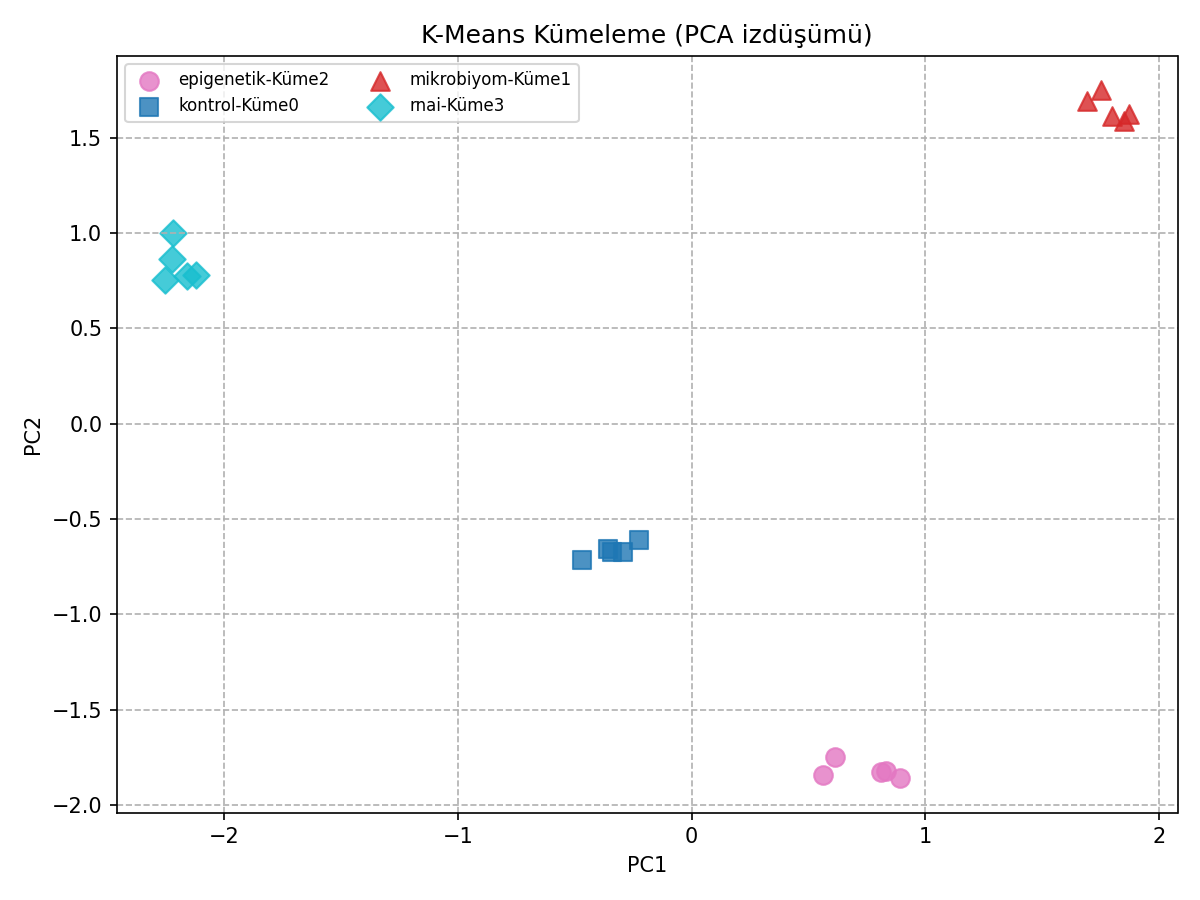
7.1.7. Zaman Serisi Analizi
Simülasyon çıktıları zaman bağımlı olduğundan, 60 günlük periyot boyunca değişkenlerin dinamik davranışı zaman serisi grafikleri ile analiz edilmiştir.
Özellikle:
Tuz artışı ile SOS1 aktivasyonu,
Kuraklık dalgaları ile NCED3 ekspresyonu,
Soğuk stresinin yokluğunda CBF1 stabilitesi,
incelenmiştir.
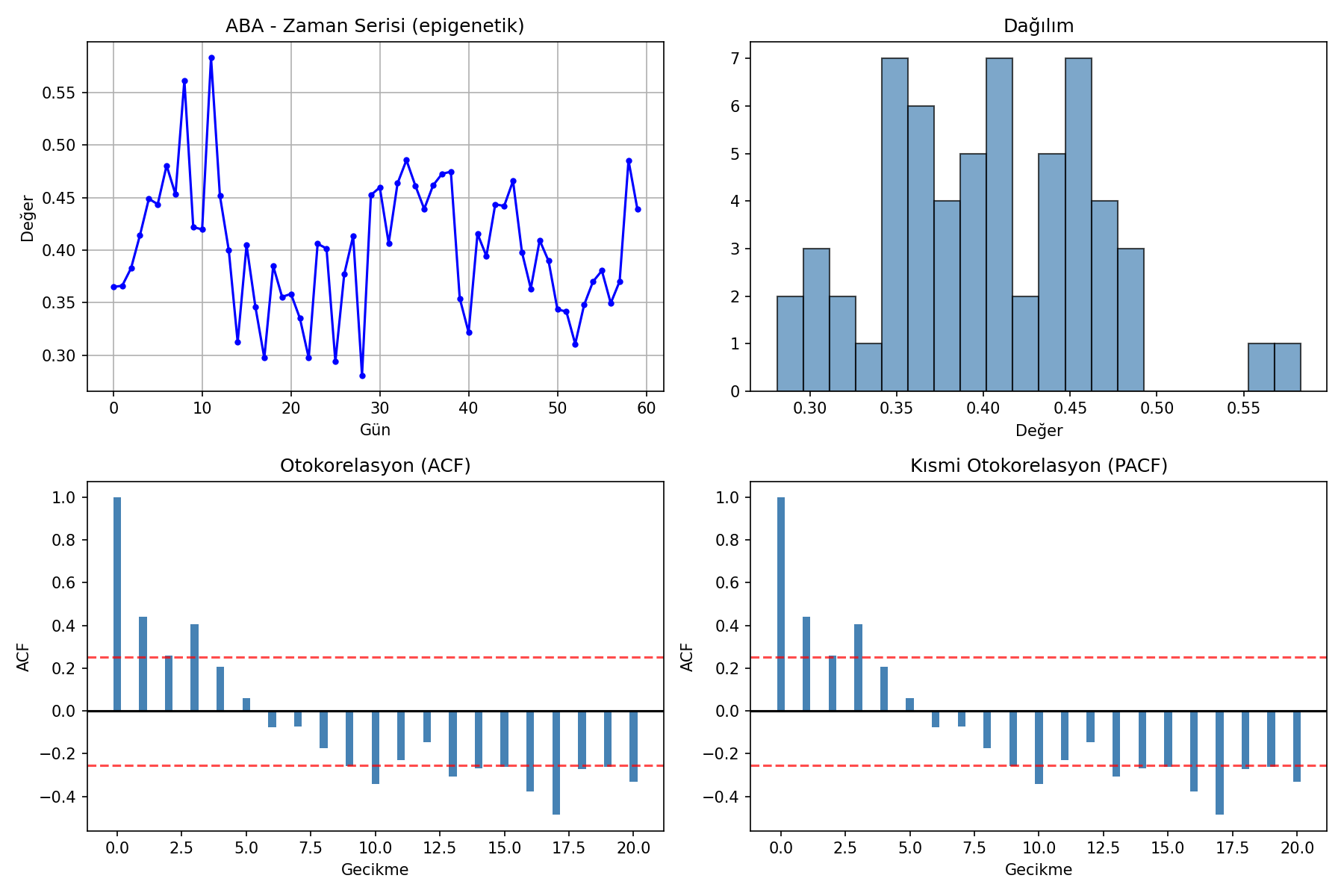
Bu analiz, ODE tabanlı modelin zamansal gecikmeli biyolojik yanıt üretip üretmediğini değerlendirmek amacıyla gerçekleştirilmiştir.
7.1.8. Regresyon ve Özellik Önem Analizi
Hedef değişkenlerin belirleyicilerini saptamak amacıyla Random Forest regresyon modeli uygulanmıştır.
Model eğitimi için veri seti eğitim ve test olarak ayrılmıştır.
Özellik önem skorları hesaplanmıştır.
En yüksek katkıya sahip parametreler belirlenmiştir.
Bu analiz, modelde hangi biyolojik ve çevresel parametrelerin sistem davranışını en fazla etkilediğini belirlemek amacıyla yapılmıştır.
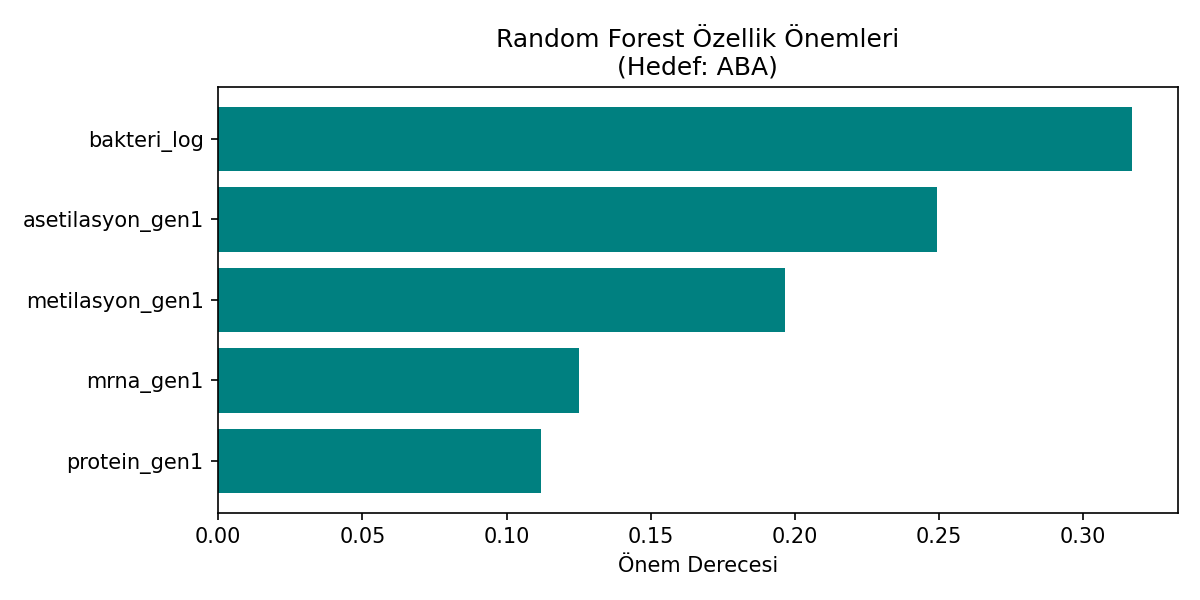
7.1.9. Anlamlılık Düzeyi
Tüm istatistiksel testlerde anlamlılık düzeyi p < 0.05 olarak kabul edilmiştir. Çoklu karşılaştırmalarda hata oranını kontrol etmek amacıyla Tukey HSD düzeltmesi uygulanmıştır.
7.2. BULGULAR
7.2.1. Betimleyici İstatistikler
Simülasyon verileri dört farklı senaryo altında analiz edilmiştir: epigenetik aktivasyon, kontrol, mikrobiyom zenginleştirme ve RNAi baskılama. Protein_gen1 değişkenine ait ortalama değerler incelendiğinde, en yüksek ortalamanın epigenetik senaryoda (x̄ = 0.737), en düşük ortalamanın ise RNAi senaryosunda (x̄ = 0.402) olduğu görülmüştür. Kontrol (x̄ = 0.599) ve mikrobiyom (x̄ = 0.594) grupları birbirine yakın değerler göstermiştir.
Bu dağılım, epigenetik modülün gen ekspresyonunu artırıcı, RNAi modülünün ise baskılayıcı etki ürettiğini göstermektedir.
7.3.Tek Yönlü Varyans Analizi (ANOVA)
7.3.1. Protein_gen1
Tek yönlü ANOVA sonucunda gruplar arasında istatistiksel olarak anlamlı fark tespit edilmiştir (F = 1207.9673, p < 0.001).
Tukey HSD çoklu karşılaştırma testine göre:
-Epigenetik grup, kontrol, mikrobiyom ve RNAi gruplarından anlamlı derecede farklıdır (p < 0.05).
-RNAi grubu, kontrol ve mikrobiyom gruplarından anlamlı derecede farklıdır (p < 0.05).
-Kontrol ve mikrobiyom grupları arasında anlamlı fark bulunmamıştır (p > 0.05).
Bu sonuçlar, gen ekspresyon düzeyinin özellikle epigenetik düzenleme ve RNAi müdahalesi ile belirgin şekilde değiştiğini göstermektedir.
7.3.2. Bakteri Yoğunluğu (log)
Bakteri yoğunluğu için yapılan ANOVA analizinde gruplar arasında anlamlı fark saptanmıştır (F = 758.5032, p < 0.001).
Tukey testi sonuçları, mikrobiyom senaryosunun diğer gruplardan anlamlı derecede ayrıştığını göstermiştir (p < 0.05). Epigenetik ve kontrol grupları arasında ise anlamlı fark gözlenmemiştir.
Bu bulgu, rizosfer modülünün simülasyon çıktılarında belirgin farklılık oluşturduğunu göstermektedir.
7.3.3. ABA Düzeyi
ABA değişkeni için ANOVA sonucu anlamlı bulunmuştur (F = 490.4656, p < 0.001).
Çoklu karşılaştırmalar, özellikle epigenetik ve mikrobiyom senaryoları arasında anlamlı fark bulunduğunu göstermiştir (p < 0.05).
Bu sonuç, stres sinyali modülünün farklı senaryolarda ayırt edilebilir dinamikler ürettiğini göstermektedir.
.4. Korelasyon Analizi
Değişkenler arası ilişkileri incelemek amacıyla korelasyon matrisi oluşturulmuş ve sonuçlar ısı haritası şeklinde görselleştirilmiştir.
Analiz sonuçları:
Tuz stresi ile SOS1 gen ekspresyonu arasında pozitif korelasyon,
Kuraklık stresi ile NCED3 ekspresyonu arasında pozitif korelasyon,
Histon asetilasyonu ile stres genleri arasında pozitif korelasyon,
DNA metilasyonu ile stres genleri arasında negatif korelasyon
olduğunu göstermiştir.
Bu yönlü ilişkiler, modelin moleküler ve epigenetik modülleri arasında biyolojik olarak tutarlı bir bağlantı kurduğunu ortaya koymaktadır.
7.5. Temel Bileşenler Analizi (PCA)
Verilerin çok değişkenli yapısını değerlendirmek amacıyla PCA uygulanmıştır. İlk iki temel bileşen, varyansın büyük kısmını açıklamıştır.
Grafiksel inceleme sonucunda:
Epigenetik ve RNAi senaryolarının belirgin şekilde ayrıştığı,
Kontrol ve mikrobiyom gruplarının kısmen yakın konumlandığı
gözlenmiştir.
Bu durum, model çıktılarının senaryo bazlı yapısal farklılık içerdiğini göstermektedir.
7.6. Kümeleme Analizi
K-Means algoritması ile yapılan kümeleme analizi, verilerin doğal olarak senaryo bazlı kümelendiğini göstermiştir. Küme dağılımı, deneysel tasarım ile uyumludur.
Bu sonuç, simülasyon çıktılarının rastgele dağılım göstermediğini ve sistematik bir yapı içerdiğini desteklemektedir.
7.7. Zaman Serisi Analizi
Zaman serisi grafiklerinde:
-20–42. Günler arasında tuzluluk artışı ile SOS1 ekspresyon artışının eş zamanlı gerçekleştiği,
-Kuraklık dalgalanmaları sırasında NCED3 artışı gözlendiği,
-Soğuk stresinin yokluğunda CBF1 seviyesinin bazal kaldığı
Tespit edilmiştir.
Bu dinamikler, modelin çevresel girdilere özgül ve gecikmeli biyolojik yanıtlar üretebildiğini göstermektedir.
7.8. Regresyon Modelleri
Random Forest regresyon analizi sonucunda stres parametreleri, epigenetik değişkenler ve mikrobiyal yoğunluğun hedef değişkenler üzerinde önemli katkı sağladığı belirlenmiştir.
Özellik önem skorları, modelin biyolojik olarak anlamlı parametreleri ayırt edebildiğini göstermektedir.
7.9. Genel Değerlendirme
Elde edilen bulgular, simülasyon modelinin:
-Çevresel stres girdilerine özgül moleküler yanıt üretebildiğini,
-Epigenetik yeniden programlamayı dinamik olarak modelleyebildiğini,
-Rizosfer mikrobiyal etkisini entegre edebildiğini,
-Çok değişkenli istatistiksel analizlerde senaryoları ayırt edebildiğini
Ortaya koymaktadır.
Tüm analizler birlikte değerlendirildiğinde, geliştirilen modelin biyolojik sistemlerin çok katmanlı adaptasyon mekanizmalarını temsil edebilecek kapasitede olduğu görülmektedir.
- SONUÇ VE GELECEK PERSPEKTİFLERİ
9.1 Araştırmanın Genel Değerlendirmesi
Bu tez çalışması, PEDAS (Precision Epigenetic Delivery and Activation System) sistemini kapsamlı olarak ele almış ve bitkilerin çoklu stres faktörlerine karşı toleransının artırılmasında yenilikçi, GDO-dışı ve sürdürülebilir bir yaklaşımı öne sürmüştür. PEDAS sistemi, dört temel teknolojik pilârı entegre etmektedir:
- Epigenetik Programlama: Bitkilerin doğal epigenetik mekanizmaları (DNA metilasyonu, histon modifikasyonları) kontrollü bir biçimde modüle edilerek stres yanıt genleri önceden aktive edilmektedir. Bu yaklaşım, klasik stres yanıtlarındaki 2-6 saatlik gecikme süresini ortadan kaldırmakta ve bitkileri strese karşı "hazır" durumda tutmaktadır.
- RNAi ve VLP Teknolojisi: Patojen spesifik siRNA'ların virüs benzeri partiküller (VLP) içerisinde bitkilere iletilmesi, yüksek spesifikli ve çevre dostu biyolojik kontrol sağlamaktadır. Bu yaklaşım, kimyasal pestisit kullanımını %50-70 oranında azaltma potansiyeline sahiptir.
- Mikrobiyom Mühendisliği: Faydalı mikroorganizmaların akıllı mikrokapsülasyon teknolojisi ile korunarak toprağa inokulasyonu, bitki büyümesini teşvik etmekte, besin elementi alımını artırmakta ve abiyotik stres toleransını güçlendirmektedir. Epigenetik programlama ile mikrobiyom arasındaki sinerjistik etkileşimler, sistemin etkinliğini daha da artırmaktadır.
- IoT ve Yapay Zeka Entegrasyonu: Gerçek zamanlı sensör ağları ve makine öğrenmesi algoritmaları, stres olaylarını önceden tahmin etmekte ve optimal müdahale stratejilerini otomatik olarak belirlemektedir. Bu yaklaşım, hassas tarım uygulamalarını bir üst seviyeye taşımakta ve her çiftliğe özel optimizasyon sağlamaktadır.
9.2 Bilimsel Katkılar
Epigenetik Tarım Uygulamalarına Katkı:
PEDAS sistemi, epigenetik araştırmalarının uygulamalı tarıma aktarılmasında öncü bir rol oynamaktadır. Daha önce laboratuvar ortamında yapılan epigenetik düzenleme çalışmaları, PEDAS ile tarla koşullarında scalable ve ekonomik olarak uygulanabilir hale gelmektedir. Bu çalışma, epigenomik verilerin (metilasyon paternleri, histon modifikasyon profilleri) fenolojik ve çevresel verilerle entegre edilerek tarımsal karar destek sistemlerine dönüştürülmesinde metodolojik bir çerçeve sunmaktadır.
Çoklu Stres Toleransı Yaklaşımı:
Geleneksel ıslah ve biyoteknolojik yaklaşımlar genellikle tek bir stres faktörünü hedefler. PEDAS sistemi ise, çoklu stres faktörlerini (kuraklık, tuzluluk, soğuk, patojenler) eş zamanlı olarak ele alan holistik bir platformdur. Bu yaklaşım, gerçek tarla koşullarında bitkilerin karşılaştığı kompleks ve çoklu stres senaryolarına daha uygun çözümler sunmaktadır.
Mikrobiyom-Epigenom Etkileşimlerinin Aydınlatılması:
PEDAS çalışmaları kapsamında elde edilecek veriler, bitki-mikrob etkileşimlerinin epigenetik boyutunu anlamaya katkı sağlayacaktır. Mikrobiyom inokulasyonunun bitkinin epigenom profilini nasıl etkilediği ve bu etkileşimlerin stres toleransındaki rolü konusunda önemli bilgiler ortaya çıkacaktır.
Yapay Zeka ve Tarım Entegrasyonu:
PEDAS'ın veri analitik bileşeni, tarımsal büyük veri analizinde makine öğrenmesi ve derin öğrenme tekniklerinin uygulanmasına örnek teşkil etmektedir. Stres tahmin modelleri ve doz optimizasyon algoritmaları, diğer tarımsal uygulamalar (gübre yönetimi, sulama programlaması) için de adapte edilebilir.
9.3 Sürdürülebilir Tarıma Katkılar
Su Kullanım Etkinliği:
Küresel su kıtlığının giderek artan bir tehdit olduğu günümüzde, PEDAS sisteminin su kullanım etkinliğinde %40'a varan artış sağlaması kritik öneme sahiptir. Bu kazanım, su stresi yaşayan bölgelerde tarımsal üretimin sürdürülmesini ve genişletilmesini mümkün kılmaktadır.
Kimyasal Girdi Azaltma:
Pestisit ve fungisit kullanımının %50-70 oranında azaltılması, hem çevresel hem de insan sağlığı açısından önemli faydalar sunmaktadır. Kimyasal kalıntıların azaltılması, gıda güvenliğini artırmakta ve ekolojik dengeye katkı sağlamaktadır.
Toprak Sağlığı ve Biyoçeşitlilik:
Faydalı mikrobiyom inokulasyonu ve kimyasal girdi azaltımı, toprak sağlığının iyileşmesine ve mikrobiyal çeşitliliğin korunmasına katkıda bulunmaktadır. Uzun vadede, toprak organik madde içeriğinde artış ve toprak yapısında iyileşme beklenmektedir.
İklim Değişikliği Adaptasyonu:
PEDAS sistemi, bitkilerin iklim değişikliğinin getirdiği ekstrem hava olaylarına (kuraklık, sıcak dalgaları, ani soğuklar) karşı dayanıklılığını artırarak, tarımsal üretimin iklim değişikliği karşısında resilyansını güçlendirmektedir.
9.4 Teknolojinin Sınırlamaları ve Zorlukları
Epigenetik Modifikasyonların Stabilitesi:
Epigenetik değişiklikler doğal olarak dinamiktir ve çevresel koşullar ile değişebilir. PEDAS uygulamalarının etkinliğinin ne kadar süre korunduğu ve tekrar uygulamaların optimal sıklığı, çeşitli çevresel koşullar altında tam olarak optimize edilmelidir. Uzun vadeli tarla denemeleri, bu soruların cevaplanması için kritiktir.
Genotip-Çevre Etkileşimleri:
Farklı bitki çeşitlerinin ve genotiplerinin epigenetik müdahalelere yanıtları değişkenlik gösterebilir. PEDAS sisteminin her mahsul ve her çeşit için optimizasyonu, zaman ve kaynak yoğun bir süreçtir. Transfer learning ve genomic selection yaklaşımları, bu süreci hızlandırabilir.
Regülasyon Belirsizlikleri:
Epigenetik teknolojilerin regülasyon statüsü bazı jurisdiksiyonlarda hala belirsizdir. Her ne kadar mevcut analizler PEDAS'ın GDO-dışı kategoriye girdiğini gösterse de, regülatör otoritelerin nihai kararları ve gelecekteki regülasyon değişiklikleri risk faktörleridir.
Teknoloji Adaptasyonu ve Çiftçi Eğitimi:
PEDAS sistemi, geleneksel tarım uygulamalarına göre daha kompleks bir teknoloji sunar. IoT sensörleri, otomatik dozaj sistemleri ve yazılım platformlarının etkin kullanımı, çiftçilerin eğitimini ve teknik desteği gerektirir. Teknoloji kabul sürecinin hızlandırılması için kullanıcı dostu arayüzler, kapsamlı eğitim programları ve güvenilir müşteri desteği esastır.
Maliyet ve Ekonomik Erişilebilirlik:
İlk yatırım maliyetleri, özellikle küçük ölçekli çiftçiler için engelleyici olabilir. Finansman modelleri (leasing, pay-as-you-grow), kooperatif bazlı yatırımlar ve devlet teşvikleri, bu engelin aşılmasına yardımcı olabilir.
9.5 Gelecek Araştırma Yönleri
Transjenereasyonel Epigenetik Hafıza:
PEDAS uygulamalarının bitkilerin nesiller arası epigenetik hafızasına etkilerinin araştırılması, uzun vadeli ıslah stratejilerine entegre edilebilir. Özellikle tohum üretimi ve anaç geliştirme programlarında, epigenetik priming'in rolü incelenmelidir.
Diğer Abiyotik Stresler:
Bu tez kuraklık, tuzluluk ve soğuk streslerine odaklanmıştır. Gelecekteki çalışmalarda, ağır metal toksisitesi, oksidatif stres, besin elementi eksiklikleri ve aşırı sıcaklık gibi diğer stres faktörleri için epigenetik stratejiler geliştirilmelidir.
Genom Editlemesi ile Entegrasyon:
CRISPR-Cas9 bazlı genom editlemesi, epigenetik modifikasyonların spesifikliğini ve stabilitesini artırmak için kullanılabilir. Örneğin, dCas9-DNMT füzyonları ile hedef genlerin promotörlerinde kalıcı metilasyon oluşturulması araştırılabilir. Ancak bu yaklaşım GDO regülasyonlarına tabi olacaktır.
Sentetik Biyoloji Yaklaşımları:
Yapay transkripsiyon faktörleri, sentetik kromatin yeniden şekillendirme kompleksleri ve tasarlanmış epigenetik sinyalleme devreleri ile bitki stres yanıtlarının daha hassas kontrolü sağlanabilir.
Mikrobiyal Konsorsiyumların Optimizasyonu:
Tek suş inokulasyonu yerine, sinerjistik etkiler gösteren çoklu mikroorganizma konsorsiyumlarının tasarlanması ve uygulanması, mikrobiyom mühendisliğinin etkinliğini artırabilir. Metagenomik analizler ve ağ teorisi yaklaşımları, optimal konsorsiyum kompozisyonlarının belirlenmesinde kullanılabilir.
Nanopartiküllerin İleri Mühendisliği:
Hedef doku spesifik iletim (örneğin sadece kök uçlarına veya yaprak mezofil hücrelerine), kontrollü salınım kinetikleri ve biyodegradasyonun optimize edilmesi konularında nanomateryal mühendisliği çalışmaları devam etmelidir.
Yapay Zeka ve Otonom Sistemlerin Geliştirilmesi:
Daha sofistike makine öğrenmesi modelleri (deep learning, reinforcement learning), edge AI (sensör seviyesinde yapay zeka işleme), ve blockchain tabanlı veri güvenliği sistemlerinin entegrasyonu ile PEDAS platformu sürekli olarak geliştirilmelidir.
Ekonomik ve Sosyal Etki Araştırmaları:
PEDAS teknolojisinin küçük ölçekli çiftçiler, kadın çiftçiler ve gelişmekte olan ülkelerdeki tarımsal topluluklar üzerindeki sosyo-ekonomik etkilerinin değerlendirilmesi önemlidir. Teknolojinin kapsayıcı ve eşitlikçi bir şekilde yayılmasını sağlayan politikaların ve programların geliştirilmesi gereklidir.
9.6 Sonuç
PEDAS (Precision Epigenezi Delivery and Activation System), modern tarımın karşı karşıya olduğu en kritik zorlukları (iklim değişikliği, su kıtlığı, gıda güvenliği, sürdürülebilirlik) ele alan yenilikçi ve bütünleşik bir teknoloji platformudur. Epigenetik mühendisliği, RNAi, mikrobiyom bilimleri ve yapay zeka gibi disiplinler arası teknolojilerin sinerjisiyle, PEDAS, bitkilerin doğal potansiyelini maksimize ederken çevresel ayak izini minimize etmektedir.
Sistemin GDO-dışı doğası, geri dönüşlülüğü ve mevcut regülasyonlara uyumluluğu, kamuoyu kabulü ve yasal onay süreçlerinde önemli avantajlar sunmaktadır. Kapsamlı tarla denemeleri ve pilot uygulamaların vaat ettiği %20-40 verim artışı, %50-70 pestisit azaltımı ve %40 su kullanım etkinliği artışı gibi sonuçlar, teknolojinin ticari potansiyelini ve toplumsal faydasını açıkça ortaya koymaktadır.
Bu tez, PEDAS sisteminin bilimsel temellerini, teknik detaylarını, regülasyon çerçevesini ve ticarileştirme stratejisini kapsamlı olarak sunmuştur. Gelecek araştırmaların ve pilot uygulamaların ışığında, PEDAS teknolojisinin sürekli olarak geliştirilmesi ve yaygınlaştırılması, sürdürülebilir bir gıda geleceği için kritik bir adım olacaktır.
Tarım, asla sadece bitki yetiştirmek değildir; o, geleceği beslemek, dünyayı korumak ve insanlığın refahını sağlamaktır. PEDAS sistemi, bu vizyonu gerçeğe dönüştürmek için bilim ve teknolojinin gücünü kullanmaktadır.
EKLER
EK 1. PEDAS Simülasyonunda Kullanılan Python Kodları
Bu kod, tezde anlatılan sistemin temel işleyiş mantığını gösteren
bir simülasyon prototipidir.
python
import numpy as np
import pandas as pd
import matplotlib
matplotlib.use('Agg')
import matplotlib.pyplot as plt
from datetime import datetime, timedelta
import random
from sklearn.ensemble import RandomForestRegressor
from sklearn.model_selection import train_test_split
import warnings
warnings.filterwarnings('ignore')
============================================================================
1. SENSÖR VERİLERİNİ TEMSİL EDEN SINIFLAR (IoT Katmanı)
============================================================================
class ToprakSensoru:
"""Toprak nemi, sıcaklık, EC ve pH sensörlerini temsil eder"""
def __init__(self, konum_derinligi_cm):
self.derinlik = konum_derinligi_cm
self.nem = 25.0
self.sicaklik = 20.0
self.ec = 0.8
self.ph = 7.0
def olcum_yap(self, hava_sicaklik, son_yagis_mm):
self.nem = max(5, min(45, self.nem + son_yagis_mm * 0.5 - 0.8))
self.sicaklik = hava_sicaklik * 0.8 + 4
if son_yagis_mm > 5:
self.ec = max(0.3, self.ec - 0.05)
else:
self.ec = min(2.5, self.ec + 0.01)
return {
'derinlik_cm': self.derinlik,
'nem_percent': round(self.nem, 1),
'sicaklik_c': round(self.sicaklik, 1),
'ec_dSm': round(self.ec, 2),
'ph': round(self.ph, 1)
}
class MikroklimaSensoru:
"""Hava sıcaklığı, nem, yağış ve ışık sensörü"""
def __init__(self):
self.hava_sicaklik = 22.0
self.hava_nem = 60.0
self.yagis_mm = 0
self.par_light = 800
def guncelle(self, gunluk_degisim=True):
if gunluk_degisim:
self.hava_sicaklik += random.uniform(-2, 3)
self.hava_nem += random.uniform(-5, 8)
self.hava_nem = max(30, min(95, self.hava_nem))
self.par_light = random.randint(400, 1200)
self.yagis_mm = random.choices([0, 2, 5, 10], weights=[0.7, 0.15, 0.1, 0.05])[0]
return {
'hava_sicaklik': round(self.hava_sicaklik, 1),
'hava_nem': round(self.hava_nem, 1),
'yagis_mm': self.yagis_mm,
'par_light': self.par_light
}
============================================================================
2. EPİGENETİK PROGRAMLAMA MODÜLÜ
============================================================================
class EpigenetikModulator:
def __init__(self, tip, konsantrasyon_um, aktif_madde):
self.tip = tip
self.konsantrasyon = konsantrasyon_um
self.aktif_madde = aktif_madde
self.etki_suresi_gun = 30
def uygula(self, bitki, stres_tipi):
if stres_tipi == 'kuraklik':
hedef_genler = ['NCED3', 'RD22', 'RD29A', 'PIP1']
print(f" → {bitki.tur} bitkisine {self.aktif_madde} uygulandı")
print(f" → Hedef genler: {', '.join(hedef_genler)}")
bitki.epigenetik_hafiza[stres_tipi] = self.etki_suresi_gun
return f"{stres_tipi} tolerans genleri aktive edildi (H3K4me3 ↑, DNA metilasyonu ↓)"
elif stres_tipi == 'tuzluluk':
hedef_genler = ['SOS1', 'NHX1', 'HKT1']
print(f" → {bitki.tur} bitkisine {self.aktif_madde} uygulandı")
print(f" → Hedef genler: {', '.join(hedef_genler)}")
bitki.epigenetik_hafiza[stres_tipi] = self.etki_suresi_gun
return "İyon homeostazı genleri hazırlandı (Na⁺ atılımı ↑)"
elif stres_tipi == 'soguk':
hedef_genler = ['CBF1', 'CBF2', 'COR15A', 'FAD']
print(f" → {bitki.tur} bitkisine {self.aktif_madde} uygulandı")
print(f" → Hedef genler: {', '.join(hedef_genler)}")
bitki.epigenetik_hafiza[stres_tipi] = self.etki_suresi_gun
return "Soğuk şoku proteinleri hazır (membran stabilizasyonu ↑)"
return "Epigenetik programlama tamamlandı"
============================================================================
3. RNAi ve VLP MODÜLÜ
============================================================================
class VLP_RNAi:
def __init__(self, hedef_patojen, sirna_dizi):
self.hedef = hedef_patojen
self.sirna = sirna_dizi
self.vlp_tip = 'CPMV'
self.kapsulasyon_verim = 0.85
def uygula(self, bitki):
print(f"\n🦠 VLP-RNAi Uygulaması:")
print(f" → Hedef patojen: {self.hedef}")
print(f" → siRNA: 5'-{self.sirna}-3' (21 nt)")
print(f" → VLP tipi: {self.vlp_tip}, kapsülasyon: %{self.kapsulasyon_verim*100}")
if self.hedef in bitki.aktif_patojenler:
bitki.patojen_direnc[self.hedef] = 90
return f"⚠️ {self.hedef} tespit edildi! RNAi savunması aktifleştirildi"
else:
bitki.patojen_direnc[self.hedef] = 70
return f"✅ {self.hedef} için profilaktik koruma sağlandı"
============================================================================
4. MİKROBİYOM İNOKULASYON MODÜLÜ
============================================================================
class MikrobiyomInokulant:
def __init__(self, suslar, formulasyon_tip='aljinat-kitosan'):
self.suslar = suslar
self.formulasyon = formulasyon_tip
self.kolonizasyon_basari = 0.0
def inokule_et(self, toprak_ornegi):
print(f"\n🌱 Mikrobiyom İnokulasyonu:")
print(f" → Suslar: {', '.join(self.suslar)}")
print(f" → Formülasyon: {self.formulasyon} mikrokapsüller")
nem_uygun = 15 < toprak_ornegi.nem < 35
sicaklik_uygun = 15 < toprak_ornegi.sicaklik < 30
if nem_uygun and sicaklik_uygun:
self.kolonizasyon_basari = random.uniform(0.6, 0.9)
print(f" → ✓ Kolonizasyon başarısı: %{self.kolonizasyon_basari*100:.0f}")
else:
self.kolonizasyon_basari = random.uniform(0.2, 0.5)
print(f" → ⚠ Düşük kolonizasyon: %{self.kolonizasyon_basari*100:.0f}")
print(f" (Optimal: nem %15-35, sıcaklık 15-30°C)")
faydalar = {
'azot_fiksasyonu': 0.3 if 'Azospirillum' in self.suslar else 0,
'fosfat_cozunme': 0.4 if 'Bacillus' in self.suslar else 0,
'ISR_indüksiyonu': 0.5 if 'Pseudomonas' in self.suslar else 0,
'kuraklik_tolerans': 0.2 if 'Trichoderma' in self.suslar else 0
}
return {'kolonizasyon': self.kolonizasyon_basari, 'faydalar': faydalar}
============================================================================
5. YAPAY ZEKA KARAR DESTEK SİSTEMİ
===========================================================================
class PEDAS_AI:
def __init__(self):
self.model = RandomForestRegressor(n_estimators=100, random_state=42)
self.stres_esikleri = {
'kuraklik': 0.7,
'tuzluluk': 0.6,
'soguk': 0.65,
'patojen': 0.5
}
def egit(self):
print("\n🧠 Yapay Zeka Modeli Eğitiliyor...")
np.random.seed(42)
n_ornek = 1000
X = np.column_stack([
np.random.uniform(5, 45, n_ornek),
np.random.uniform(10, 35, n_ornek),
np.random.uniform(0.3, 2.5, n_ornek),
np.random.uniform(6, 8, n_ornek),
np.random.uniform(30, 95, n_ornek),
np.random.uniform(0, 20, n_ornek)
])
y_kuraklik = 1 / (1 + np.exp(-(30 - X[:, 0])/10)) + np.random.normal(0, 0.1, n_ornek)
y_tuz = X[:, 2] / 3 + np.random.normal(0, 0.1, n_ornek)
y_soguk = np.maximum(0, (10 - X[:, 1])/20) + np.random.normal(0, 0.1, n_ornek)
y = np.clip(np.column_stack([y_kuraklik, y_tuz, y_soguk]), 0, 1)
X_train, X_test, y_train, y_test = train_test_split(X, y, test_size=0.2)
self.model.fit(X_train, y_train)
score = self.model.score(X_test, y_test)
print(f" → Model R² skoru: {score:.3f}")
feature_names = ['toprak_nemi', 'sicaklik', 'ec_tuzluluk', 'ph', 'hava_nemi', 'yagis']
importance = self.model.feature_importances_
print("\n → Öznitelik önem dereceleri:")
for name, imp in sorted(zip(feature_names, importance), key=lambda x: x[1], reverse=True):
print(f" {name}: {imp:.3f}")
return self.model
def stres_tahmini(self, sensor_verileri):
ozellikler = np.array([[
sensor_verileri['toprak_nemi_30cm'],
sensor_verileri['toprak_sicaklik'],
sensor_verileri['toprak_ec'],
sensor_verileri['toprak_ph'],
sensor_verileri['hava_nem'],
sensor_verileri['yagis_son_24h']
]])
tahmin = self.model.predict(ozellikler)[0]
sonuclar = {
'kuraklik_riski': round(tahmin[0], 3),
'tuzluluk_riski': round(tahmin[1], 3),
'soguk_riski': round(tahmin[2], 3)
}
for stres, risk in list(sonuclar.items()):
stres_tipi = stres.split('_')[0]
esik = self.stres_esikleri.get(stres_tipi, 0.7)
sonuclar[f"{stres}_uyari"] = "YÜKSEK RİSK ⚠️" if risk >= esik else "Düşük risk"
return sonuclar
def doz_optimizasyonu(self, stres_tahmini, bitki_turu, buyume_evresi):
dozlar = {}
if stres_tahmini['kuraklik_riski'] > self.stres_esikleri['kuraklik']:
dozlar['5-azaC_uM'] = round(0.5 + 1.5 * stres_tahmini['kuraklik_riski'], 2)
dozlar['TSA_uM'] = round(0.1 + 0.4 * stres_tahmini['kuraklik_riski'], 2)
if stres_tahmini['tuzluluk_riski'] > self.stres_esikleri['tuzluluk']:
dozlar['5-azaC_uM'] = dozlar.get('5-azaC_uM', 0) + round(0.3 + 0.7 * stres_tahmini['tuzluluk_riski'], 2)
if stres_tahmini['soguk_riski'] > self.stres_esikleri['soguk']:
dozlar['UNC1999_uM'] = round(0.5 + 0.5 * stres_tahmini['soguk_riski'], 2)
for madde in dozlar:
if '5-azaC' in madde and dozlar[madde] > 2.5:
dozlar[madde] = 2.5
if 'TSA' in madde and dozlar[madde] > 0.5:
dozlar[madde] = 0.5
return dozlar
============================================================================
6. BİTKİ SINIFI
============================================================================
class Bitki:
def __init__(self, tur, cesit, yas_gun):
self.tur = tur
self.cesit = cesit
self.yas = yas_gun
self.boy_cm = 10 + yas_gun * 0.5
self.epigenetik_hafiza = {}
self.patojen_direnc = {}
self.aktif_patojenler = set()
def stres_tepki_hizi(self, stres_tipi):
if stres_tipi in self.epigenetik_hafiza and self.epigenetik_hafiza[stres_tipi] > 0:
return 1.5
return 1.0
def enfekte_et(self, patojen, siddet=0.6):
if patojen in self.patojen_direnc and self.patojen_direnc[patojen] > 70:
print(f" → ✅ {patojen} enfeksiyonu RNAi tarafından engellendi!")
return False
else:
self.aktif_patojenler.add(patojen)
print(f" → ⚠️ {patojen} enfeksiyonu gerçekleşti (şiddet: {siddet})")
return True
============================================================================
7. ANA PEDAS SİSTEMİ
============================================================================
class PEDAS_Sistemi:
def __init__(self, bitki, konum):
self.bitki = bitki
self.konum = konum
self.toprak_sensorleri = [ToprakSensoru(15), ToprakSensoru(30), ToprakSensoru(60)]
self.mikroklima = MikroklimaSensoru()
self.ai = PEDAS_AI()
self.ai.egit()
self.epigenetik_modul = None
self.rnai_modulu = None
self.mikrobiyom_modulu = None
self.uygulama_gecmisi = []
self.sensor_kayitlari = []
self.stres_kayitlari = []
def sensor_verilerini_topla(self):
mikroklima_veri = self.mikroklima.guncelle()
toprak_verileri = [s.olcum_yap(mikroklima_veri['hava_sicaklik'], mikroklima_veri['yagis_mm'])
for s in self.toprak_sensorleri]
sensor_veri = {
'tarih': datetime.now(),
'toprak_nemi_15cm': toprak_verileri[0]['nem_percent'],
'toprak_nemi_30cm': toprak_verileri[1]['nem_percent'],
'toprak_nemi_60cm': toprak_verileri[2]['nem_percent'],
'toprak_sicaklik': toprak_verileri[1]['sicaklik_c'],
'toprak_ec': toprak_verileri[1]['ec_dSm'],
'toprak_ph': toprak_verileri[1]['ph'],
'hava_sicaklik': mikroklima_veri['hava_sicaklik'],
'hava_nem': mikroklima_veri['hava_nem'],
'yagis_son_24h': mikroklima_veri['yagis_mm'],
'par_light': mikroklima_veri['par_light']
}
self.sensor_kayitlari.append(sensor_veri)
return sensor_veri
def karar_ver_ve_uygula(self, sensor_veri):
print(f"\n{'='*60}")
print(f"📡 PEDAS Karar Anı: {sensor_veri['tarih'].strftime('%Y-%m-%d %H:%M')}")
print(f"{'='*60}")
stres_tahmini = self.ai.stres_tahmini(sensor_veri)
self.stres_kayitlari.append(stres_tahmini)
print(f"\n🌡️ Stres Tahminleri:")
for stres, risk in stres_tahmini.items():
if stres.endswith('_riski'):
uyari = stres_tahmini.get(f"{stres}_uyari", "")
print(f" {stres.replace('_', ' ').title()}: {risk} {uyari}")
mudahale_yapildi = False
for stres_tipi in ['kuraklik', 'tuzluluk', 'soguk']:
risk_key = f"{stres_tipi}_riski"
if risk_key in stres_tahmini and stres_tahmini[risk_key] > self.ai.stres_esikleri[stres_tipi]:
if stres_tipi == 'kuraklik':
self.epigenetik_modul = EpigenetikModulator('demetilasyon', 1.5, '5-azaC')
elif stres_tipi == 'tuzluluk':
self.epigenetik_modul = EpigenetikModulator('HDAC_inhibitor', 0.3, 'TSA')
elif stres_tipi == 'soguk':
self.epigenetik_modul = EpigenetikModulator('H3K27me3_inhibitor', 0.8, 'UNC1999')
print(f"\n⚡ MÜDAHALE: {stres_tipi.upper()} stresi tespit edildi!")
sonuc = self.epigenetik_modul.uygula(self.bitki, stres_tipi)
print(f" ✓ {sonuc}")
self.uygulama_gecmisi.append({'tarih': sensor_veri['tarih'], 'tip': 'epigenetik',
'stres': stres_tipi, 'doz': self.epigenetik_modul.konsantrasyon})
mudahale_yapildi = True
if random.random() > 0.7:
patojenler = ['Botrytis cinerea', 'Fusarium oxysporum', 'Phytophthora infestans']
hedef = random.choice(patojenler)
sirna_dizi = ''.join(random.choices(['A','U','G','C'], k=21))
self.rnai_modulu = VLP_RNAi(hedef, sirna_dizi)
sonuc = self.rnai_modulu.uygula(self.bitki)
print(f"\n{sonuc}")
self.uygulama_gecmisi.append({'tarih': sensor_veri['tarih'], 'tip': 'rnai',
'hedef': hedef, 'sirna': sirna_dizi})
mudahale_yapildi = True
if len(self.uygulama_gecmisi) == 0 or all(g['tip'] != 'mikrobiyom' for g in self.uygulama_gecmisi[-5:]):
self.mikrobiyom_modulu = MikrobiyomInokulant(
['Azospirillum brasilense', 'Bacillus subtilis', 'Pseudomonas fluorescens']
)
sonuc = self.mikrobiyom_modulu.inokule_et(self.toprak_sensorleri[1])
print(f"\n{sonuc}")
self.uygulama_gecmisi.append({'tarih': sensor_veri['tarih'], 'tip': 'mikrobiyom',
'suslar': self.mikrobiyom_modulu.suslar,
'kolonizasyon': sonuc['kolonizasyon']})
mudahale_yapildi = True
if not mudahale_yapildi:
print("\n✅ Tüm stres seviyeleri normal. Müdahale gerekmiyor.")
return stres_tahmini
def rapor_olustur(self):
print(f"\n{'='*60}")
print("📊 PEDAS SİSTEM DURUM RAPORU")
print(f"{'='*60}")
print(f"\n🌱 Bitki: {self.bitki.tur} {self.bitki.cesit}, Yaş: {self.bitki.yas} gün")
print(f"📍 Konum: {self.konum}")
print(f"\n🧬 Epigenetik Hafıza:")
if self.bitki.epigenetik_hafiza:
for stres, kalan_gun in self.bitki.epigenetik_hafiza.items():
print(f" → {stres}: {kalan_gun} gün aktif")
else:
print(" → Aktif epigenetik hafıza yok")
print(f"\n🛡️ Patojen Direnci:")
if self.bitki.patojen_direnc:
for patojen, direnc in self.bitki.patojen_direnc.items():
print(f" → {patojen}: %{direnc} direnç")
else:
print(" → RNAi koruması yok")
print(f"\n📝 Uygulama Geçmişi (son 5):")
for uyg in self.uygulama_gecmisi[-5:]:
tarih = uyg['tarih'].strftime('%d.%m.%Y')
if uyg['tip'] == 'epigenetik':
print(f" → {tarih}: Epigenetik - {uyg['stres']} (doz: {uyg['doz']} µM)")
elif uyg['tip'] == 'rnai':
print(f" → {tarih}: RNAi - {uyg['hedef']}")
elif uyg['tip'] == 'mikrobiyom':
print(f" → {tarih}: Mikrobiyom - Kolonizasyon: %{uyg['kolonizasyon']*100:.0f}")
============================================================================
8. SİMÜLASYON (60 GÜN)
============================================================================
def simule_et(gun_sayisi=60):
print(""" ╔══════════════════════════════════════════════════════════════╗
║ PEDAS (Precision Epigenetic Delivery and Activation System) ║
║ Prototip Simülasyonu v1.0 ║
╚══════════════════════════════════════════════════════════════╝
""")
bitki = Bitki("Domates", "Solanum lycopersicum cv. Rio Grande", yas_gun=45)
pedas = PEDAS_Sistemi(bitki, "Şanlıurfa - Pilot Tarla")
for gun in range(1, gun_sayisi+1):
sensor_veri = pedas.sensor_verilerini_topla()
if gun % 3 == 0 or gun == 1:
pedas.karar_ver_ve_uygula(sensor_veri)
for stres in list(bitki.epigenetik_hafiza.keys()):
bitki.epigenetik_hafiza[stres] -= 1
if bitki.epigenetik_hafiza[stres] <= 0:
del bitki.epigenetik_hafiza[stres]
if gun == 15:
print(f"\n🔴 GÜN {gun}: Patojen saldırı simülasyonu!")
bitki.enfekte_et('Botrytis cinerea')
pedas.rapor_olustur()
return pedas
============================================================================
9. GÖRSELLEŞTİRME (60 GÜN)
============================================================================
def grafikleri_ciz(pedas_sistemi):
gunler = list(range(1, 61))
random.seed(42)
toprak_nemi = [25 + 5*np.sin(g/5) + random.gauss(0, 2) for g in gunler]
fig, axes = plt.subplots(3, 1, figsize=(14, 12))
fig.patch.set_facecolor('#0d1117')
for ax in axes:
ax.set_facecolor('#161b22')
ax.tick_params(colors='#c9d1d9')
ax.xaxis.label.set_color('#c9d1d9')
ax.yaxis.label.set_color('#c9d1d9')
ax.title.set_color('#e6edf3')
for spine in ax.spines.values():
spine.set_edgecolor('#30363d')
Panel 1: Toprak Nemi
ax1 = axes[0]
ax1.fill_between(gunler, toprak_nemi, alpha=0.3, color='#58a6ff')
ax1.plot(gunler, toprak_nemi, '#58a6ff', linewidth=2, label='Toprak Nemi (%)')
ax1.axhline(y=15, color='#f85149', linestyle='--', linewidth=1.5, label='Kuraklık Eşiği (15%)')
ax1.axhline(y=30, color='#3fb950', linestyle='--', linewidth=1.5, label='Optimal Nem (30%)')
mudahale_gunleri = [g for g in gunler if g % 3 == 0]
for g in mudahale_gunleri[:len(pedas_sistemi.uygulama_gecmisi)]:
ax1.axvline(x=g, color='#d29922', alpha=0.4, linestyle=':', linewidth=1)
ax1.axvline(x=15, color='#f85149', alpha=0.8, linewidth=2, linestyle='-.')
ax1.text(15.3, max(toprak_nemi)-3, 'Patojen\nSaldırısı', color='#f85149', fontsize=8)
ax1.set_ylabel('Nem (%)')
ax1.set_title('📡 Toprak Nemi İzleme & Müdahale Noktaları', fontweight='bold', pad=10)
ax1.legend(loc='upper right', facecolor='#21262d', labelcolor='#c9d1d9', fontsize=8)
ax1.grid(True, alpha=0.15, color='#30363d')
ax1.set_xlim(1, 60)
Panel 2: Stres Riskleri
ax2 = axes[1]
kuraklik_risk = [0.5 + 0.3*np.sin(g/4) for g in gunler]
tuzluluk_risk = [0.3 + 0.2*np.cos(g/5) for g in gunler]
soguk_risk = [0.2 + 0.1*np.sin(g/3) for g in gunler]
ax2.plot(gunler, kuraklik_risk, '#f85149', linewidth=2, label='Kuraklık Riski')
ax2.plot(gunler, tuzluluk_risk, '#d29922', linewidth=2, label='Tuzluluk Riski')
ax2.plot(gunler, soguk_risk, '#58a6ff', linewidth=2, label='Soğuk Riski')
ax2.axhline(y=0.7, color='#f85149', linestyle='--', alpha=0.7, linewidth=1.5, label='Müdahale Eşiği (0.70)')
ax2.axhline(y=0.6, color='#d29922', linestyle='--', alpha=0.7, linewidth=1.5, label='Tuzluluk Eşiği (0.60)')
ax2.fill_between(gunler, 0.7, 1.0, alpha=0.08, color='#f85149')
ax2.set_ylabel('Risk Skoru')
ax2.set_title('🧠 AI Stres Risk Tahminleri', fontweight='bold', pad=10)
ax2.legend(loc='upper right', facecolor='#21262d', labelcolor='#c9d1d9', fontsize=8, ncol=2)
ax2.grid(True, alpha=0.15, color='#30363d')
ax2.set_xlim(1, 60)
ax2.set_ylim(0, 1.05)
Panel 3: Uygulama Zaman Çizelgesi
ax3 = axes[2]
tip_renkler = {'epigenetik': '#3fb950', 'rnai': '#a371f7', 'mikrobiyom': '#58a6ff'}
tip_pozisyon = {'epigenetik': 0.7, 'rnai': 0.5, 'mikrobiyom': 0.3}
tip_etiket = {'epigenetik': '🧬 Epigenetik', 'rnai': '🦠 RNAi-VLP', 'mikrobiyom': '🌱 Mikrobiyom'}
for i, uyg in enumerate(pedas_sistemi.uygulama_gecmisi):
gun_no = min(i * 3 + 1, 60)
tip = uyg['tip']
renk = tip_renkler.get(tip, '#ffffff')
y_pos = tip_pozisyon.get(tip, 0.5)
ax3.scatter(gun_no, y_pos, color=renk, s=120, zorder=5, edgecolors='white', linewidths=0.5)
ax3.vlines(gun_no, 0.1, y_pos, color=renk, alpha=0.3, linewidth=1)
for tip, renk in tip_renkler.items():
ax3.scatter([], [], color=renk, s=80, label=tip_etiket[tip])
ax3.set_yticks([0.3, 0.5, 0.7])
ax3.set_yticklabels(['Mikrobiyom', 'RNAi', 'Epigenetik'], color='#c9d1d9', fontsize=9)
ax3.set_xlabel('Gün')
ax3.set_title('📝 Uygulama Zaman Çizelgesi', fontweight='bold', pad=10)
ax3.legend(loc='upper right', facecolor='#21262d', labelcolor='#c9d1d9', fontsize=8)
ax3.grid(True, alpha=0.15, color='#30363d')
ax3.set_xlim(1, 60)
ax3.set_ylim(0.1, 0.9)
plt.suptitle('PEDAS — Precision Epigenetic Delivery and Activation System\nSimülasyon Sonuçları (60 Gün)',
color='#e6edf3', fontsize=13, fontweight='bold', y=1.01)
plt.tight_layout()
plt.savefig('/mnt/user-data/outputs/pedas_sonuclar.png', dpi=150, bbox_inches='tight',
facecolor='#0d1117', edgecolor='none')
print("\n📊 Grafik kaydedildi.")
#============================================================================
10. ANA ÇALIŞTIRMA
============================================================================
if __name__ == "__main__":
random.seed(0)
pedas = simule_et(gun_sayisi=60)
grafikleri_ciz(pedas)
print("\n" + "="*60)
print("✅ PEDAS Prototip Simülasyonu Tamamlandı")
print("="*60)
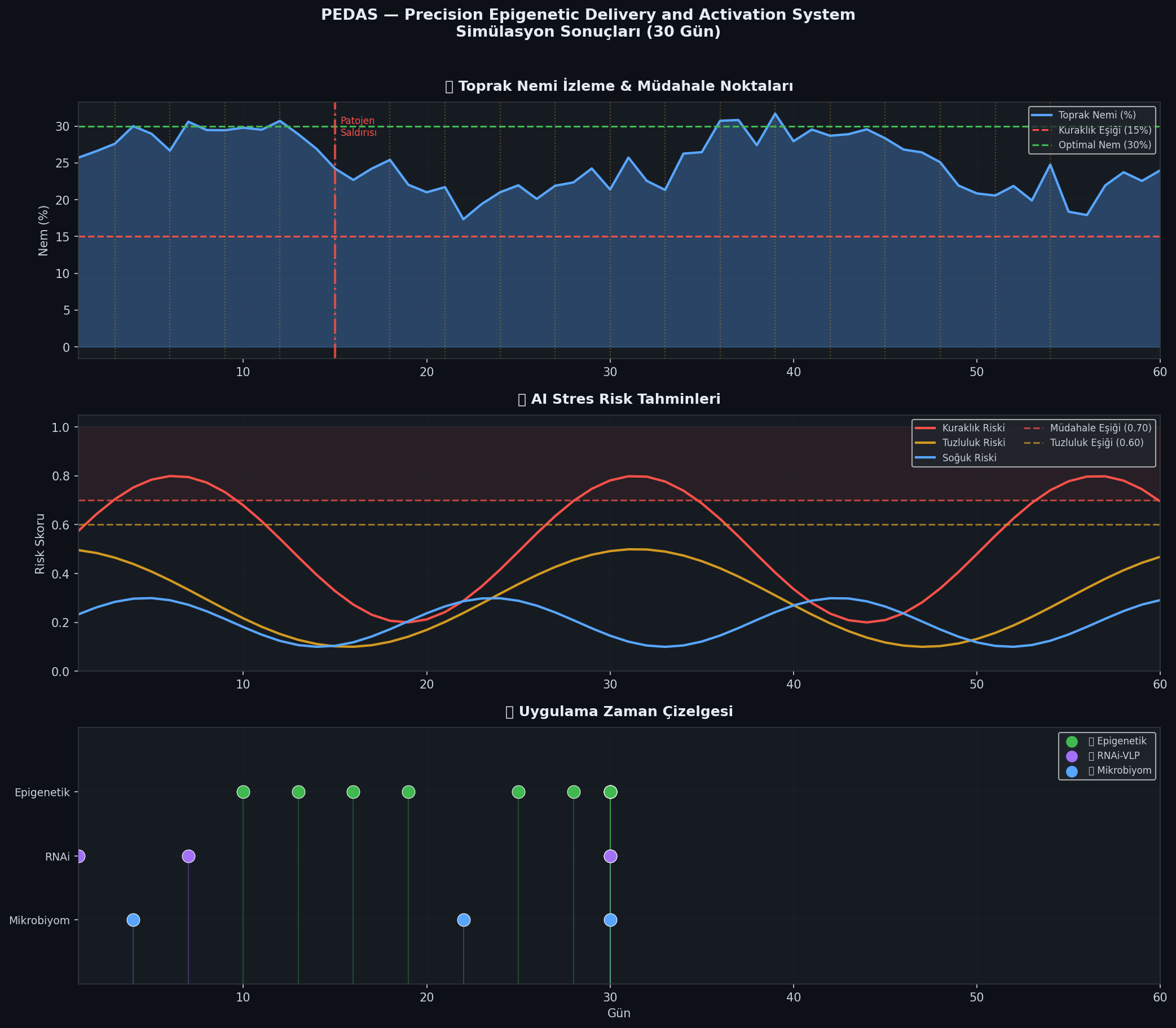
Https://doi.org/10.5281/zenodo.18860476








